
Аннотация
Данный конспект посвящён основным направлениям нанобологии и нанотехнологий. В нем отражены наиболее интересные и перспективные достижения фундаментальной биологии, которые могут найти отражения в нанотехнологиях.
В конспекте: 24 страницы, 2 таблицы, 2 иллюстрации.
Ключевые слова: наноструктуры, нанопроцессы, наноявления, нанотехнологии.
Глоссарий
Нанобиотехнологии – раздел в нанотехнологиях, посвященный изучению воздействия наночастиц на живые системы, а также разработке способов применения биологических наноструктур и нанопроцессов в медицине, экологии, сельском хозяйстве и других отраслях производства. Нанотехнологии – фундаментальные технологии, основанные на манипуляциях с наноструктурами.
Наноявления – явления живой природы, протекающие с участием наноструктур.
Нанопроцессы – процессы, в которые вовлекаются наноструктуры (наночастицы).
Белок – высокомолекулярное органическое соединение, построенное из остатков аминокислот и играющее первостепенную роль в процессах жизнедеятельности всех живых организмов.
Комплементарность – свойство азотистых оснований образовывать с помощью водородных связей парные комплексы (аденин-тимин или аденин-урацил, гуанин-цитозин) при взаимодействии цепей нуклеиновых кислот.
Биомакромолекулы – молекулы биополимеров (нуклеиновых кислот, белков, полисахаридов)
Модификация белков – химические превращения полипептида: разрезание молекулы на фрагменты; сшивание отдельных фрагментов полипептида в новую молекулу; соединение простых белков с разнообразными веществами с образованием сложных белков – гликопротеинов, липопротеинов, металлопротеинов и др.; химические превращения отдельных аминокислот в составе полипептида (окисление, образование дисульфидных и водородных связей).
Оглавление
Введение 6
1. Основные направления и задачи нанобиотехнологий 9
1.1 Основные направления 9
1.2 Классификация задач нанобиотехнологий 9
1.3 Процессы в биотехнологии 10
2. Нанотехнологии на основе ДНК 11
2.1 Создание нанороботов 11
2.2 Искуственные наноматериалы на основе ДНК 12
3. Биомакромолекулы как составляющие наномира 12
3.1 Конструирование наноструктур на основе белков 12
3.2. Изучение рецепторной функции мембраны и разработка новых нанобиотехнологий 13
3.3. Нанобиосенсоры, их применение в диагностике и лечении заболеваний 14
4. Нанобиотехнологии на основе метода генетической инженерии 17
4.1. Генетическая инженерия как одно из направлений нанобиотехнологий 17
4.2. Биоинженерия в животноводстве 18
Заключение 21
Список литературы......................................................................................... 22
Введение
«Из атомов мы будем собирать все – от лекарств до космического лифта».
Эрик Дрекслер, «гуру» нанотехнологий.
Век биологии или век исчезновения человечества! Только таким может стать XXI век по мнению многих ученых, требующих незамедлительно объявить начавшее отсчет столетие веком биологии. Однако смена «века физики» «веком биологии», предрекавшаяся последние десятилетия XX века, к сожалению, еще не состоялась. Вполне возможно, что ожидаемый прорыв в биологических исследованиях обеспечат стремительно развивающиеся нанобиология и нанобиотехнологии. Под нанотехнологиями понимают фундаментальные технологии, основанные на манипуляциях с наноструктурами (наночастицами). Наноструктуры – это объекты, размеры которых лежат в диапазоне от 1 до 100 нанометров.
Нанобиотехнологии – раздел в нанотехнологиях, посвященный изучению воздействия наночастиц на живые системы, а также разработке способов моделирования и практического применения биологических наноструктур, наноявлений и нанопроцессов1.

Рисунок 1. Направления бионанотехнологий
 Фактически бионанотехнологии означают попытку совместить биологические молекулы, системы живой клетки и созданные человеком наноструктуры – живое с неживым. Уникальность природы всегда вдохновляла и завораживала человека, искушала его повторить совершенство биологических структур и механизмов в искусственно создаваемых системах. Вот и сейчас популярность биологических подходов в нанотехнологиях вызвана стремлением создавать уникальные микромашины, осуществлять сборку сложных наноструктур из составных блоков, доставку и разделение наночастиц и компонентов смесей – все то, что уже миллионы лет реализуется в природных системах (Рис. 1). Одна из наиболее острых проблем, стоящих перед человеком, – это проблема старения, решить которую безуспешно пытались на протяжении многих веков, изобретая эликсиры молодости и чудодейственные снадобья. Поэтому особое место в бионанотехнологиях занимают материалы для медицины 3. Фактически бионанотехнологии означают попытку совместить биологические молекулы, системы живой клетки и созданные человеком наноструктуры – живое с неживым. Уникальность природы всегда вдохновляла и завораживала человека, искушала его повторить совершенство биологических структур и механизмов в искусственно создаваемых системах. Вот и сейчас популярность биологических подходов в нанотехнологиях вызвана стремлением создавать уникальные микромашины, осуществлять сборку сложных наноструктур из составных блоков, доставку и разделение наночастиц и компонентов смесей – все то, что уже миллионы лет реализуется в природных системах (Рис. 1). Одна из наиболее острых проблем, стоящих перед человеком, – это проблема старения, решить которую безуспешно пытались на протяжении многих веков, изобретая эликсиры молодости и чудодейственные снадобья. Поэтому особое место в бионанотехнологиях занимают материалы для медицины 3.
1. Основные направления и задачи нанобиотехнологий
«Настоящий автор нанотехнологий - Ганс Христиан Андерсен (Голый Король)».
Аноним.
1.1 Основные направления
Фундаментальные исследования в области нанотехнологий направлены на познание биологических, химических, физических свойств и явлений наномира. Кроме того, они предусматривают разработку способов комбинирования этих свойств при производстве новых материалов и создании новых технологий. Открытия в области наноисследований уже успешно используются в биотехнологиях, медицине, электронике, транспорте, сельском хозяйстве, охране окружающей среды и других отраслях экономики. Нанотехнологии органически объединяют последние достижения всех естественных наук, создавая основу новой технологической революции. Последняя предусматривает переход от работы с веществом к манипуляциям с отдельными атомами, молекулами и их комплексами. Основные направления развития нанобиотехнологий можно объединить в три группы:
• моделирование и воспроизведение наноявлений и наномеханизмов живых систем в лабораторных и производственных условиях;
• получение наночастиц и наноматериалов с участием живых организмов;
• использование наноструктур и нанопроцессов для вторжения в живой организм с целью его исследования, диагностики состояния и лечения [1].
1.2 Классификация задач нанобиотехнологий и процессов
Конкретными задачами нанобиотехнологий в настоящее время считаются:
• решение фундаментальных биологических проблем, нерешенных с помощью традиционных цитологических и цитохимических методик (моделирование биологических процессов, анализ поведения биомолекул и атомно-молекулярных комплексов живых клеток, мониторинг жизнедеятельности отдельных клеток);
• изучение взаимодействия наночастиц с молекулами ДНК с целью разработки новых методов генетической инженерии;
• изучение механизмов транспорта веществ через биологические мембраны с применением наночастиц и создание нанотехнологий направленной доставки лекарств;
• разработка биосенсорных систем для биологии и медицины с целью выявления определенного вещества в окружающей среде или организме человека, а также для обнаружения мутаций;
• изучение возможностей применения наночастиц в качестве новых наноматериалов медицинского назначения: сорбенты для выведения из организма или удаления с его поверхности нежелательных и токсичных соединений (продукты метаболизма, тяжелые металлы, радионуклиды, ксенобиотики);
• создание новых высокочувствительных и удобных в применении систем для диагностики и эффективного лечения заболеваний на самых ранних стадиях развития;
• разработка и создание на основе нанобиочастиц нанотехнологий и наноматериалов для выделения белков, их модификации и последующего производства белковых препаратов;
• разработка самовопроизводящихся систем на основе биоаналогов – бактерий, вирусов, простейших животных;
• изучение влияния наночастиц на сложноорганизованные биологические системы, включая организмы животных и человека;
• разработка на основе нанобиотехнологий лекарственных препаратов нового поколения;
• создание биологически совместимых (неотторгаемых организмом) медицинских материалов для пересадки в живой организм;
• разработка нанороботов, способных устранять возникающие в органах очаги поражения, и не провоцирующих иммунные реакции [1].
1.3 Процессы в биотехнологии
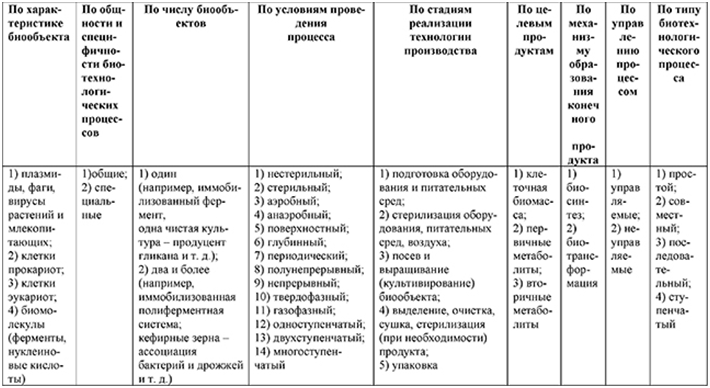
Важной задачей в создании любого биотехнологического процесса является разработка и оптимизация научно-обоснованной технологии и аппаратуры для него. При организации биотехнологических производств частично был заимствован опыт развитой к тому времени химической технологии. Однако биотехнологические процессы имеют существенные отличия от химических, поскольку в биотехнологии используют более сложную организацию материи - биологическую. Каждый биологический объект (клетка, фермент и т. д.) - это автономная саморегулирующаяся система. Природа биологических процессов сложна и далеко не выяснена окончательно. Для микробных популяций, например, характерна существенная гетерогенность по ряду признаков - возрасту, физиологической активности, устойчивости к воздействию неблагоприятных факторов среды. Они также подвержены случайным мутациям, частота которых составляет 10-4-10-8. Гетерогенность также может быть обусловлена наличием поверхностей раздела фаз и неоднородностью среды. В основу подразделения биотехнологических процессов могут быть положены различные принципы, например, оценка принадлежности объектов к надцарствам живых существ, функциональной активности биообъекта, возможности вычленения отдельных этапов из биотехнологических схем производства в виде самостоятельных процессов: выделение, очистка и упаковка готового продукта и т.д. (табл. 1).
Таблица 1. Систематизация биотехнологических процессов
2. Нанотехнологии на основе ДНК
«Биосистемы – это самые совершенные системы на свете, а бионанотехнологии – это попытка воспроизвести их». Дж. Райан
2.1 Создание нанороботов
 Можно ли создать из ДНК наноробот? К тому же автономно (самостоятельно) передвигающийся и останавливающийся? Утвердительный ответ был дан группой ученых из Колумбийского университета (США). Им удалось создать автономный молекулярный робот из ДНК и белка, способный перемещаться, менять направление движения и останавливаться. Эта разработка получила название наноробот «Паук» . Можно ли создать из ДНК наноробот? К тому же автономно (самостоятельно) передвигающийся и останавливающийся? Утвердительный ответ был дан группой ученых из Колумбийского университета (США). Им удалось создать автономный молекулярный робот из ДНК и белка, способный перемещаться, менять направление движения и останавливаться. Эта разработка получила название наноробот «Паук» .
Каким же образом была решена проблема автономного передвижения наноробота? Исследователи использовали свойство полинуклеотидной цепочки ДНК связываться посредством водородных связей с другой комплементарной ей цепочкой. Поэтому ходильные конечности (ноги) наноробота были сконструированы из ДНК. Тело наноробота «Паук» формировалось из белка под названием «стрептавидин». Длина наноробота составила 4 нанометра . Три из четырех ног «Паука» сделаны из молекул ДНК, способных связываться с определенной последовательностью другой молекулы ДНК и вырезать ее. Четвертая нога представляет собой своеобразный якорь, который привязывается к начальной точке на треке. Робот запускается с места своего старта специальной цепочкой ДНК. Связывая и затем вырезая участки ДНК, находящиеся за пределами основной цепочки, робот передвигается по треку. Несмотря на то, что первые подобные нанороботы появились еще несколько лет назад, им не удавалось сделать более 3 шагов. Наноробот «Паук» может пройти примерно 100 нанометров (25 размеров самого паука или 50 его шагов). Это расстояние он проходит за 30-60 минут. За «Пауком» ученые смогли наблюдать благодаря атомно-силовым микроскопам. С помощью таких микроскопов было установлено, что нанороботов можно отправлять по четырем различным направлениям. В настоящее время исследователи приступили к решению самой серьезной проблемы в рамках их многолетнего проекта: научиться управлять поведением нанороботов и «научить» несколько «Пауков» работать вместе, взаимодействуя друг с другом. В отдаленной перспективе подобные нанороботы смогут, по мнению ученых, очищать мельчайшие капилляры и уничтожать раковые клетки в живом организме.
2.2 Искуственные наноматериалы на основе ДНК
 Все возрастающие масштабы пересадки (трансплантации) привели к острому дефициту донорских органов и биологических тканей. Как никогда ранее стала актуальной проблема создания совершенных искусственных биологических тканей, свойства которых были бы максимально близки к природным. Все возрастающие масштабы пересадки (трансплантации) привели к острому дефициту донорских органов и биологических тканей. Как никогда ранее стала актуальной проблема создания совершенных искусственных биологических тканей, свойства которых были бы максимально близки к природным.
Группе исследователей из Австралии и Кореи под руководством Д.Спинкса удалось найти один из вариантов решения задачи. Они разработали для целей трансплантации новый материал, механические свойства которого подобны свойствам биологических тканей. Созданный материал представляет собой прочную композитную систему из спиралей ДНК и углеродных нанотрубок (рис. 2).

Рисунок 2. Схема получения нановолокон
Спиралями ДНК полностью «обертывают» углеродные нанотрубки и помещают их в специальную жидкость, содержащую ионы кальция. В такой жидкости из обернутых спиралями ДНК углеродных нанотрубок формируется гелеобразная масса. Полученный гель можно спрясть в волокна так же, как прядут синтетические волокна. После высушивания волокна из нанотрубок и ДНК обретают форму сети из скрученных нановолокон толщиной 50 нанометров (рис. 2). Каждое волокно имеет при этом пористую губкообразную структуру.
Получаемые искусственные нановолокна близки по своим свойствам к белковым волокнам, обеспечивающим прочность и эластичность таких органов как сухожилия, мышцы, артерии, кожа. Поэтому искусственные нановолокна из ДНК и углеродных нанотрубок несомненно найдут широкое применение при изготовлении самых разнообразных искусственных имплантантов 1.
3. Биомакромолекулы как составляющие наномира
3.1. Конструирование наноструктур на основе белков
Образующиеся белковые наноструктуры чрезвычайно разнообразны по форме (трехмерной структуре) и размерам. Разнообразие является следствием: во-первых, большого количества аминокислотных остатков в молекуле полипептида (от нескольких десятков до нескольких сотен), во-вторых, способностью каждого такого остатка приобретать около 10 пространственных конфигураций и вступать в разнообразные связи с другими молекулами белка. Примечательно то, что в живом организме форма и размеры исходных белковых наноблоков более строго определяют форму и структуру надмолекулярных комплексов, чем в искусственных условиях. Это обстоятельство заинтересовало наноконструкторов и нанотехнологов. Используя такие отличия поведения белковых молекул в искусственных условиях, можно получать практически любые необходимые наноструктуры (нанокомплексы) на основе белка. Даже такие, которые никогда не возникают в живых организмах. Получаемые белковые наноструктуры можно выделять из среды, очищать и кристаллизовать. Затем их можно изучать, используя весь арсенал физических и химических методов, включая оптическую, ультрафиолетовую, инфракрасную спектроскопию с высоким временным разрешением. Результаты изучения белковых надмолекулярных структур используются при конструировании нанокомплексов и наноагрегатов в лабораторных и производственных условиях. Рассмотрим первые достижения подобных работ. Можно ли с помощью белковых молекул наладить автоматическую сборку наночастиц? Первыми утвердительный ответ на этот вопрос дали российские ученые из Института биоорганической химии РАН. Они разработали технологию автоматической сборки  наночастиц с помощью молекул белков барнас и барстар. Упомянутые белки были выделены из палочкообразных бактерий. Этим двум видам белков была отведена роль «роботов» на сборочной линии. Наночастицы, собранные таким образом, представляют интерес как для медицины, так и для новых биотехнологий. К наночастицам можно присоединять молекулы лекарственных препаратов, радиоактивные изотопы для диагностики и лечения раковых заболеваний. В наночастицу можно вмонтировать радиоактивный изотоп, флуоресцентную частицу, лекарства, токсины. Как белковыми наночастицами заменить антибиотики? В первую очередь те антибиотики, к которым у микроорганизмов уже выработалась устойчивость? К решению такой проблемы первыми приступили исследователи из Института биоинженерии и нанотехнологий Сингапура. Они обратили внимание на катионные белки – белки, которые в растворе обретают положительный заряд. На основе молекул этих белков исследователи создали самособирающиеся наночастицы . Такие наночастицы обладают антимикробным действием и могут заменять традиционные антибиотики. При этом белковые наночастицы действуют сразу на множество микроорганизмов и уничтожают даже те, которые выработали устойчивость против большинства современных антибиотиков1. наночастиц с помощью молекул белков барнас и барстар. Упомянутые белки были выделены из палочкообразных бактерий. Этим двум видам белков была отведена роль «роботов» на сборочной линии. Наночастицы, собранные таким образом, представляют интерес как для медицины, так и для новых биотехнологий. К наночастицам можно присоединять молекулы лекарственных препаратов, радиоактивные изотопы для диагностики и лечения раковых заболеваний. В наночастицу можно вмонтировать радиоактивный изотоп, флуоресцентную частицу, лекарства, токсины. Как белковыми наночастицами заменить антибиотики? В первую очередь те антибиотики, к которым у микроорганизмов уже выработалась устойчивость? К решению такой проблемы первыми приступили исследователи из Института биоинженерии и нанотехнологий Сингапура. Они обратили внимание на катионные белки – белки, которые в растворе обретают положительный заряд. На основе молекул этих белков исследователи создали самособирающиеся наночастицы . Такие наночастицы обладают антимикробным действием и могут заменять традиционные антибиотики. При этом белковые наночастицы действуют сразу на множество микроорганизмов и уничтожают даже те, которые выработали устойчивость против большинства современных антибиотиков1.
3.2. Изучение рецепторной функции мембраны и разработка новых нанобиотехнологий
В исследованиях рецепторной функции клеточной мембраны особо перспективным является изучение рецепторов, формируемых трансмембранными белками под названием GPCR. Это обусловлено тем, что около трети всех производимых лекарств оказывают воздействие на клетки лишь после того, как провзаимодействуют с их белками-рецепторами GPCR. Поэтому эффективность применения многих лекарств зависит от того, смогут ли они связаться с локализованными в клеточных мембранах белками GPCR. Как обеспечить связывание создаваемого лекарственного препарата с белками-рецепторами GPCR? Решение проблемы поначалу казалось несложным. Поскольку лекарство будет выступать в роли лиганда, необходимо добиться максимального соответствия между ним и участком узнавания лиганда, имеющимся у рецептора. Для этого необходимо знать пространственную структуру белка-рецептора. Однако изучение конфигурации белков-рецепторов оказалось очень трудным и безрезультатным: после извлечения из клеточной мембраны трансмембранные белки-рецепторы сразу же утрачивали свою естественную конфигурацию. Те немногие белки-рецепторы, трехмерную структуру которых все же удалось определить, оказались неподходящими рецепторами для молекул лекарственных препаратов. Возможен ли иной подход к решению проблемы определения пространственной конфигурации белка-рецептора?
Он был найден в лаборатории биологических систем Технологического института штата Джорджия (США). Группа исследователей под руководством Джефри Сколника просто смоделировала структуру белков-рецепторов, используя компьютер. Для этого была применена специальная компьютерная программа TASSER, разработанная исследователями в 2004 году. Программа TASSER позволяет на основе последовательности аминокислот в белковой молекуле предсказывать с высокой точностью ее пространственную (трехмерную) конфигурацию. В качестве исходных данных были взяты генетические коды 907 белков GPCR, не превышающих по длине 500 аминокислот. Для 820 из них удалось получить модели, пригодные для использования в дальнейших исследованиях. В перспективе в лаборатории планируется моделирование молекул различных лекарств и изучение их взаимодействия с трансмембранными белками-рецепторами1.
3.3. Нанобиосенсоры, их применение в диагностике и лечении заболеваний
 На основе механизмов функционирования белков-переносчиков и белков-рецепторов учеными разработаны нанобиосенсоры. Они позволяют осуществлять высокочувствительное выявление специфических белков, вирусов или ДНК в органах, тканях, клетках и биологических жидкостях. Конструктивно нанобиосенсор представляет собой комбинированное устройство, состоящее из двух преобразователей – биохимического и физического, находящихся в тесном контакте друг с другом . На основе механизмов функционирования белков-переносчиков и белков-рецепторов учеными разработаны нанобиосенсоры. Они позволяют осуществлять высокочувствительное выявление специфических белков, вирусов или ДНК в органах, тканях, клетках и биологических жидкостях. Конструктивно нанобиосенсор представляет собой комбинированное устройство, состоящее из двух преобразователей – биохимического и физического, находящихся в тесном контакте друг с другом .
 Каким образом кристаллический белок можно применить в нанобиосенсорах? Исследователи удалили белковый S-слой с поверхности бактерии и разбили его на «субъединицы». Поместив затем субъединицы в раствор, они добились объединения их в кристаллическую решетку, формируемую уже на кремниевых, металлических и синтетических подложках. К помещенному на подложку S-слою были добавлены специальные сенсорные молекулы, которые вместе со слоем сформировали точный биоаналитический сенсор. Подобным образом австрийскими исследователями был создан сенсор глюкозы на основе S-слоя и молекулы фермента оксидазы глюкозы. Во время реакции фермента с глюкозой, через нанобиосенсор проходит электрический ток. Измеряемая величина тока характеризует содержание глюкозы. Как скажется на свойствах нанопровода размещение на его поверхности белков-рецепторов? Поиск ответа на этот вопрос завершился созданием нанобиосенсоров иного типа (рис. 6). В таком нанобиосенсоре на поверхность нанопровода нанесен слой специальных белков-рецепторов (сенсорных молекул). Последние обладают способностью специфически связываться с биологическими макромолекулами. В результате образования такой связи изменяется электрическая проводимость нанопровода. Эти изменения сигнализируют о выявлении определенного вещества. В настоящее время на основе нанопроводов создан уникальный нанобиосенсор, позволяющий выявлять единичные вирусы. Связывание вируса со специфическим белкомрецептором (антителом), нанесенным на поверхность нанопровода, вызывает значимое изменение электрической проводимости. Однако на этом исследователи не остановились. Можно ли сконструировать нанобиосенсор, способный одновременно выявлять сразу несколько видов вирусов? Ученые разместили на поверхности одного нанопровода несколько различных белков-рецепторов (антител), чувствительных к различным видам вирусов. При связывании с белками-рецепторами любого из этих вирусов регистрируется изменение проводимости нанопровода. Тем самым определяется присутствие вируса. Такие устройства, несомненно, найдут широкое применение в медицинской диагностике. Особого внимания заслуживают наносенсоры, которые выявляют последовательность нуклеотидов в ДНК. В одном из таких уже созданных устройств рецепторы, нанесенные на нанопровода, способны обнаруживать мутантные гены, вызывающие заболевание муковисцидоз. Всем известно значение как можно более раннего выявления раковых заболеваний. Для успешного их лечения важно выявить первые появившиеся раковые клетки в органе. Возможно ли обнаружение единичных злокачественных клеток с помощью нанобиосенсоров? Ответом на этот вопрос стало создание нанобиосенсоров на основе углеродных нанотрубок. Известно, что в ответ на появление в организме чужеродных веществ, называемых антигенами, иммунная система вырабатывает антитела. Последние представляют собой специфические глобулярные белки. Каждый вид антител избирательно взаимодействует с определенным антигеном (белковым рецептором). Ученые попытались применить антитела, специфичные к рецепторам (антигенам) мембраны раковых клеток. Ими они покрыли углеродные нанотрубки. Получившиеся нанобиосенсоры способны обнаруживать злокачественные клетки в организме и определять вид опухоли. Кроме диагностики заболеваний нанобиосенсоры могут найти применение в направленном транспорте лекарственных веществ к клеткаммишеням. В настоящее время создаются наноконтейнеры (липосомы, мицеллы, полимерные наночастицы), поверхность которых покрыта специальными сенсорными молекулами (своеобразными антителами), обеспечивающими возможность найти клетку-мишень в любой части организма. Внутрь наноконтейнера могут помещаться молекулы лекарственного вещества или, например, ген, кодирующий белок, который запускает процесс самоуничтожения клетки. При связывании антител с рецепторами «больных» клеток содержимое контейнера перемещается внутрь клетки, что приводит к «выздоровлению» больных клеток или гибели раковых клеток. Таким образом, наибольший интерес для медицины представляют два направления использования нанобиосенсоров в совокупности с наноконтейнерами: 1) обнаружение антител, специфичных к антигенам больных клеток; 2) избирательная доставки лекарственных средств непосредственно к больным клеткам. Использование медикаментозных препаратов, заключенных в наночастицы, сводит до минимума их разрушение и утрату активности по пути к больному органу. При этом предотвращается возникновение нежелательных побочных явлений, а также возрастает эффективность применения препарата1.Нанобиосенсоры могут быть запрограммированы на обнаружение в биологических жидкостях (слюна, кровь и др.) комплекса белков, являющихся индикаторами развития тех или иных заболеваний. Ученые полагают, что нанобиосенсоры способны внести революционные изменения в медицинскую диагностику заболеваний. Какие же свойства белков способствовали их применению в создаваемых нанобиосенсорах? Исследователи из наноцентра в Вене (Австрия) обратили внимание на свойство некоторых белков образовывать регулярные структуры в виде кристаллических решеток . Многие бактерии, в частности, формируют на своей поверхности одномолекулярные слои кристаллического белка , называемые S-слоями. Каким образом кристаллический белок можно применить в нанобиосенсорах? Исследователи удалили белковый S-слой с поверхности бактерии и разбили его на «субъединицы». Поместив затем субъединицы в раствор, они добились объединения их в кристаллическую решетку, формируемую уже на кремниевых, металлических и синтетических подложках. К помещенному на подложку S-слою были добавлены специальные сенсорные молекулы, которые вместе со слоем сформировали точный биоаналитический сенсор. Подобным образом австрийскими исследователями был создан сенсор глюкозы на основе S-слоя и молекулы фермента оксидазы глюкозы. Во время реакции фермента с глюкозой, через нанобиосенсор проходит электрический ток. Измеряемая величина тока характеризует содержание глюкозы. Как скажется на свойствах нанопровода размещение на его поверхности белков-рецепторов? Поиск ответа на этот вопрос завершился созданием нанобиосенсоров иного типа (рис. 6). В таком нанобиосенсоре на поверхность нанопровода нанесен слой специальных белков-рецепторов (сенсорных молекул). Последние обладают способностью специфически связываться с биологическими макромолекулами. В результате образования такой связи изменяется электрическая проводимость нанопровода. Эти изменения сигнализируют о выявлении определенного вещества. В настоящее время на основе нанопроводов создан уникальный нанобиосенсор, позволяющий выявлять единичные вирусы. Связывание вируса со специфическим белкомрецептором (антителом), нанесенным на поверхность нанопровода, вызывает значимое изменение электрической проводимости. Однако на этом исследователи не остановились. Можно ли сконструировать нанобиосенсор, способный одновременно выявлять сразу несколько видов вирусов? Ученые разместили на поверхности одного нанопровода несколько различных белков-рецепторов (антител), чувствительных к различным видам вирусов. При связывании с белками-рецепторами любого из этих вирусов регистрируется изменение проводимости нанопровода. Тем самым определяется присутствие вируса. Такие устройства, несомненно, найдут широкое применение в медицинской диагностике. Особого внимания заслуживают наносенсоры, которые выявляют последовательность нуклеотидов в ДНК. В одном из таких уже созданных устройств рецепторы, нанесенные на нанопровода, способны обнаруживать мутантные гены, вызывающие заболевание муковисцидоз. Всем известно значение как можно более раннего выявления раковых заболеваний. Для успешного их лечения важно выявить первые появившиеся раковые клетки в органе. Возможно ли обнаружение единичных злокачественных клеток с помощью нанобиосенсоров? Ответом на этот вопрос стало создание нанобиосенсоров на основе углеродных нанотрубок. Известно, что в ответ на появление в организме чужеродных веществ, называемых антигенами, иммунная система вырабатывает антитела. Последние представляют собой специфические глобулярные белки. Каждый вид антител избирательно взаимодействует с определенным антигеном (белковым рецептором). Ученые попытались применить антитела, специфичные к рецепторам (антигенам) мембраны раковых клеток. Ими они покрыли углеродные нанотрубки. Получившиеся нанобиосенсоры способны обнаруживать злокачественные клетки в организме и определять вид опухоли. Кроме диагностики заболеваний нанобиосенсоры могут найти применение в направленном транспорте лекарственных веществ к клеткаммишеням. В настоящее время создаются наноконтейнеры (липосомы, мицеллы, полимерные наночастицы), поверхность которых покрыта специальными сенсорными молекулами (своеобразными антителами), обеспечивающими возможность найти клетку-мишень в любой части организма. Внутрь наноконтейнера могут помещаться молекулы лекарственного вещества или, например, ген, кодирующий белок, который запускает процесс самоуничтожения клетки. При связывании антител с рецепторами «больных» клеток содержимое контейнера перемещается внутрь клетки, что приводит к «выздоровлению» больных клеток или гибели раковых клеток. Таким образом, наибольший интерес для медицины представляют два направления использования нанобиосенсоров в совокупности с наноконтейнерами: 1) обнаружение антител, специфичных к антигенам больных клеток; 2) избирательная доставки лекарственных средств непосредственно к больным клеткам. Использование медикаментозных препаратов, заключенных в наночастицы, сводит до минимума их разрушение и утрату активности по пути к больному органу. При этом предотвращается возникновение нежелательных побочных явлений, а также возрастает эффективность применения препарата1.Нанобиосенсоры могут быть запрограммированы на обнаружение в биологических жидкостях (слюна, кровь и др.) комплекса белков, являющихся индикаторами развития тех или иных заболеваний. Ученые полагают, что нанобиосенсоры способны внести революционные изменения в медицинскую диагностику заболеваний. Какие же свойства белков способствовали их применению в создаваемых нанобиосенсорах? Исследователи из наноцентра в Вене (Австрия) обратили внимание на свойство некоторых белков образовывать регулярные структуры в виде кристаллических решеток . Многие бактерии, в частности, формируют на своей поверхности одномолекулярные слои кристаллического белка , называемые S-слоями.
4. Нанобиотехнологии на основе метода генетической инженерии
4.1. Генетическая инженерия как одно из направлений нанобиотехнологий
Современные биотехнологии трудно представить без создания новых форм организмов с желательными для человека свойствами. Каким образом можно изменить признаки и свойства живого организма (его фенотип), чтобы они сохранялись также у его потомков? Это возможно осуществить только изменяя генотип организма, т.е. его наследственный материал. Целенаправленное изменение и конструирование наследственного материала (ДНК) живых организмом является предметом генетической инженерии. Молекулы ДНК, создаваемые методами генетической инженерии, называют рекомбинантными. Раздел молекулярной биологии, связанный с созданием новых комбинаций генетического материала, способного обеспечивать биосинтез продуктов обмена веществ, получил название генетической инженерии. Кем и когда были заложены основы метода генетической инженерии? Начало генетической инженерии было положено в 1972 году, когда американский ученый П. Берг в лабораторных условиях впервые создал рекомбинантную ДНК. Последняя соединила в себе фрагменты ДНК трех организмов: вируса «SV 40», бактериофага «лямбда» и бактерии «кишечная палочка». Опыт П. Берга был бы невозможен, если бы ранее не удалось открыть два уникальных типа ферментов: 1) рестриктазы, разрезающие молекулу ДНК в строго определенных участках; 2) лигазы, соединяющие отрезки различных молекул ДНК друг с другом. Рестриктазы получили весьма удачное образное название «биологических ножей», которыми манипулируют генные инженеры, разрезая молекулы ДНК на фрагменты.
Вторым необходимым условием успешного проведения опытов по генетической инженерии стало использование «векторов». Векторы представляют собой вирусы или получаемые из бактерий короткие внехромосомные фрагменты их ДНК – плазмиды. С помощью рестриктаз и лигаз ученые встраивают в векторы необходимый фрагмент ДНК (ген). Задача вектора – внести новую ДНК (ген) в клетку и встроить ее в ДНК организма-хозяина. Совершенствование методов генетической инженерии позволило объединять генетическую информацию неродственных организмов, в том числе стоящих на разных ступенях эволюции. Кроме того, «в пробирке» (in vitro) можно управлять процессом создания рекомбинантной ДНК так, чтобы обходить запрещающие механизмы живого организма. Методы генетической инженерии успешно внедряются в производство лекарственных препаратов. На их основе уже производятся в широких масштабах инсулин, интерферон и интерлейкин. На основе генетической инженерии разработаны технологии получения трансгенных растений (рис. 7) и животных, отличающихся не только высокой урожайностью (плодовитостью), но одновременно и повышенной  устойчивостью к болезням и паразитам. Так, в Бельгии и США выведены сорта картофеля и томатов, которые устойчивы к колорадскому жуку и позволяют на 40-60% сократить применение инсектицидов. устойчивостью к болезням и паразитам. Так, в Бельгии и США выведены сорта картофеля и томатов, которые устойчивы к колорадскому жуку и позволяют на 40-60% сократить применение инсектицидов.
Какие конкретные задачи необходимо решить экспериментатору, чтобы успешно осуществить опыт по генетической инженерии? Выполнение конкретной генно-инженерной работы требует решения трех задач: 1) создать рекомбинантную ДНК, пригодную для переноса в клетку; 2) разработать метод введения рекомбинантной ДНК в клетку; 3) создать условия для нормального функционирования генов, введенных в клетку организма-хозяина. Каждая работа в области генетической инженерии выполняется в несколько этапов: 1) необходимый ген выделяют из естественных источников или синтезируют химическим путем; 2) подбирают вектор (молекулу ДНК, переносящую необходимый ген в клетку); 3) вектор и переносимый ген объединяют (рис. 8) в единую структуру (рекомбинантную молекулу ДНК); 4) единую структуру, содержащую вектор и ген, вводят в клетку организма-хозяина.
4.2. Биоинженерия в животноводстве
К настоящему моменту только два вида генетически модифицированных животных было создано для потребления в пищу человеком. Один из них — трансгенный лосось, выведенный компанией Aqua Bounty Technologies. Ген гормона роста из чавычи (чинукского лосося) был соединен с промотером. Промотер необходим для транскрипции гена. В отличие от обычной рыбы в трансгенном лососе гормон роста образуется круглый год, существенно увеличивая скорость роста рыбы. Этот признак сейчас пытаются выработать и у других рыб, выращиваемых в рыбных хозяйствах, включая форель, тилапию и палтус.
Экологи высказывают серьезные опасения, что такая биоинженерная рыба может вытеснить естественные популяции, так как рыба, выращиваемая на ферме, часто попадает в дикую природу.
Вторым трансгенным сельскохозяйственным животным является свинья Enviropig, выведенная исследователями в Гуэлфском университете (University of Guelph) штата Онтарио. В это животное введен ген фитазы, который экспрессируется в клетках слюнных желез. Фитаза расщепляет фосфаты в пище свиньи, уменьшая тем самым их содержание в помете животного. Широкое распространение этих животных может существенно снизить вредное влияние свиноферм на окружающую среду.
Ученые проводят ряд многообещающих исследований по биоинженерии пищевых продуктов, получаемых из животных. Некоторые попытки направлены на уменьшение чувствительности к болезням среди кур, овец и коров. Компания ViaGen нашла креветку, которая содержит в своем геноме гены устойчивости ко многим болезням, и отобрала животных, несущих эти гены. Создание устойчивых к болезням популяций креветки имеет серьезный потенциал влияния на Pacific Rim, где выращивание креветок — достаточно большой бизнес. Исследователи в Университете Миннесоты изучают гены индейки, которые вызывают развитие большой грудинки, и гены, связанные с устойчивостью к сальмонелле.
Как мы, люди, заинтересованы в установлении наших предков, так и фермеры-животноводы заинтересованы в биотехнологии, которая помогает установить родословную животного. Например, при разведении коров происхождение от рода Angus считается очень ценным, но трудным для сертификации. Компания ViaGen недавно подзаработала на этом, разработав генетический тест, с помощью кото рого можно высчитать процент генов от Angus, имея образец бычьей крови или ткани.
Федеральное и частное финансирование биоинженерии сельскохозяйственных животных отстает от других сельскохозяйственных инициатив. Тем не менее ряд компаний занимается выведением животных, которые растут быстрее, включая свиней, овец и индюшек. Другие направления связаны с генетическим профилированием и клонированием. Клонирование, однако, имеет очень низкую производственную эффективность (менее 2  и высокую частоту анатомических дефектов в потомстве. Одна из технологий, привлекшая внимание общества, — использование бычьего гормона роста (Bovine Growth Hormone — BGH) для увеличения скорости роста и продукции молока у крупного рогатого скота. Эта практика, однако, вызывает рост числа случаев заболевания маститом и, следовательно, требует увеличения применения антител, что вызывает опасения относительно качества молока. Кроме того, повышение содержания гормона роста укорачивает жизнь коров и способствует увеличению чувствительности отдельных животных к поранению. и высокую частоту анатомических дефектов в потомстве. Одна из технологий, привлекшая внимание общества, — использование бычьего гормона роста (Bovine Growth Hormone — BGH) для увеличения скорости роста и продукции молока у крупного рогатого скота. Эта практика, однако, вызывает рост числа случаев заболевания маститом и, следовательно, требует увеличения применения антител, что вызывает опасения относительно качества молока. Кроме того, повышение содержания гормона роста укорачивает жизнь коров и способствует увеличению чувствительности отдельных животных к поранению.
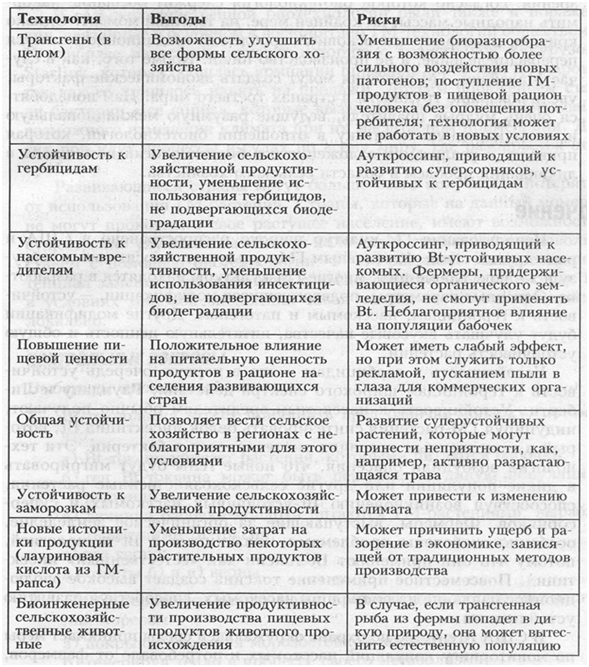
Мы можем ожидать ускорения развития биоинженерии сельскохозяйственных животных с завершением расшифровки генома кур и крупного рогатого скота. Это знание сформирует основу для быстрых изменений в животноводстве: методах разведения, размеров особей и вкуса получаемой из них продукции. В таблице 1 показаны выгоды и риски применения биотехнологии в сельском хозяйстве.
Таблица 2. Выгоды и риски применения биотехнологий в сельском хозяйстве
Заключение
Многие нанопроцессы и наноявления живой природы появились на Земле еще около 3 млрд. лет тому назад. Последующие периоды эволюции живого многократно убеждают нас в гениальности древнейшего наноконструктора и нанотехнолога планеты – Природы. Всестороннее познание живых структур и механизмов жизнедеятельности на самих глубинных уровнях организации живого – главное условие конструирования наноструктур и разработки нанотехнологий путем моделирования. Глубокое изучение живых прототипов и воссоздание их в технических моделях останется основным направлением в нанобиологии и нанобиотехнологиях на ближайшую перспективу.
Список литературы
1. Сыч В.Ф., Дрождина Е.П., Санжапова А.Ф. Введение в нанобиологию и нанобиотехнологии. Учебное пособие для учащихся 10-11 классов средних общеобразовательных учреждений. – СПб: Образовательный центр «Участие», Образовательные проекты, 2012 – 256 с. (Серия «Наношкола» 
2. Нолтинг Б. Новейшие методы исследования биосистем. М.: Техносфера, 2005. – 256 с.
3. http://medbe.ru/materials/mikrobiologiya-i-biotekhnologii/protsessy-v-biotekhnologii/ - Процессы в биотехнологии
4. http://www.rusdocs.com/bioinzheneriya-v-zhivotnovodstve - Биоинженерия в животноводстве |