Российский Университет Дружбы Народов
Инженерная академия
Кафедра кибернетики и мехатроники
Курс «Введение в наноинженерию»
"Введение в нанобиологию и нанобиотехнологии"
Студент ИИб-201 (2 курс): Вечканов А. Р.
Преподаватель: доцент Лапшинский В. А.
Москва 2016г.
Аннотация:
В рефератe рассмотрен вопрос нанотехнологий. Указана взаимосвязь нанотехнологий с биологией, генетической инженерией и медициной, а именно, применение нанотехнологий в адресной доставке лекарств, использование наносенсоров для диагностики различных заболеваний. Рассмотрено применение нанотехнологий в имплантологии. Предложены перспективы развития нанотехнологий. Отмечено, что (био)наноинженеру в области биологии клетки, развития и генетики. В приложении имеются контрольные вопросы/ответы, небольшой сборник интересных задач и заданий в области БНТ
В работе: рис. 9, стр. 22, источников 5.
Ключевые слова: нанотехнология, бионанотехнология, наноинженерия, бионаноинженерия, нанобиология.
Глоссарий терминологии, сокращения и обозначения
Нанотехнологии (НТ) ‒ это фундаментальные технологии, основанные на манипуляциях с наноструктурами (наночастицами).
Бионанотехнологии (БНТ) ‒это использование биологических строительных блоков, а также биологических специфичности и активности в развивающейся нанотехнологии.
Наноинженерия ‒научно-практическая деятельность человека по конструированию, изготовлению и применению наноразмерных (наноструктурированных) объектов или структур, а также объектов или структур, созданных методами нанотехнологий.
Бионаноинженерия ‒научно-практическая деятельность человека по конструированию, изготовлению и применению наноразмерных (наноструктурированных) биообъектов или биоструктур, а также объектов или структур, созданных методами бионанотехнологий
Нанобиология ‒раздел биологии, изучающий биологические объекты методами нанотехнологии
Содержание
Введение…………………………………………………………………………...4
1.Нанобиотехнологии и медицина………………………………………………5
2.Генетическая инженерия и нанотехнологии……………………………….....6
3.Нанотехнологии для диагностики……………………………………………..8
4.Нанотехнологии и направленная доставка лекарств………………………..10
5.Медицинские имплантаты на основе нанотехнологий………………….......12
6.Тканевая инженерия ………………………………………………………….13
7.Перспективные направление нанобиотехнологии………………………….15
Заключение……………………………………………………………………….16
Список литературы………………………………………………………………17
Приложение 1. Какая биология нужна наноинженеру
Приложение. 2. Контрольные вопросы и ответы по БНТ
Приложение. 3. Сборник задач/заданий по БНТ
Введение
Любой материальный предмет - это всего лишь
скопление атомов в пространстве.
То, как эти атомы собраны в структуру,
определяет, что это будет за предмет.
С.Лем
Физик и философ Этин Клин считает, что возможность технологического прорыва за счет нанотехнологий вполне реальна, но во многом это строится на энтузиазме ученого.
С момента экспериментального подтверждения существования атомов до момента получения возможности ими манипулировать прошло меньше 100 лет. Перед учеными открываются такие возможности, о которых раньше и подумать не могли. Только благодаря этому правительство всех развитых стран стало проявлять интерес к соответствующим наукам. Все началось с американской инициативы 2002 года, с которой выступили физики Рока и Бенбридж. Эти ученые выступили с сумасшедшей идеей о том, что благодаря нанотехнологиям человечество сможет решить все стоящие перед ним проблемы.
Это заявление стало толчком к началу многочисленных исследований, позволивших реализовать такие передовые направления науки и техники, как микроэлектроника, информатика, ядерно-энергетические исследования, микробиология, лазерная техника, медицина и многое другое.
1Нанобиотехнологии и медицина
Развитие биологии и медицины характеризовалось постепенным переходом от визуальных методов исследования к молекулярным и атомным.
Внедрение методов нанобиотехнологий в практическую медицину привели к обособлению в ней такого направления как «наномедицина». Наномедицина включает диагностику и лечение заболеваний человека на молекулярном уровне. Взаимосвязь биотехнологий, нанотехнологий и медицины показана на рисунке 1.
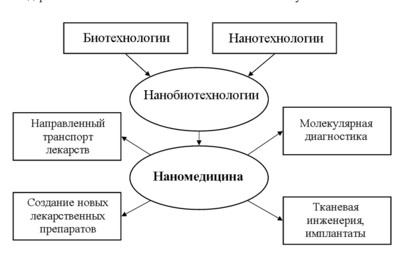
Рис. 1. Взаимосвязь биотехнологий, нанотехнологий и медицины.
Методы наномедицины предусматривают использование различных наночастиц для адресной доставки лекарств и фрагментов ДНК в нуждающиеся клетки. Нанотехнологии могут обеспечить доставку препарата не только в определенную клетку, но и в ее конкретную часть (органоид). Новые методы позволяют увеличить время действия препаратов и значительно снизить их побочные эффекты.
Нанотехнологии способствуют также усовершенствованию методов диагностики заболеваний. Использование наночастиц позволяет отыскивать в живом организме раковые и другие неблагополучные клетки [1]. Благодаря нанотехнологиям значительно повышена чувствительность методов распознавания в биохимической диагностике.
Среди основных направлений наномедицины можно выделить:
• доставку активных лекарственных веществ;
• новые методы и средства лечения нанометрового уровня;
• нанодиагностику в живом организме и лабораторных условиях (invivo и in vitro);
• тканевую инженерию;
• медицинские имплантаты [1].
2 Генетическая инженерия и нанотехнологии
Современные биотехнологии трудно представить без создания новых форм организмов с желательными для человека свойствами. Каким образом можно изменить признаки и свойства живого организма (его фенотип),чтобы они сохранялись также у его потомков? Это возможно осуществить только изменяя генотип организма, т.е. его наследственный материал. Целенаправленное изменение и конструирование наследственного материала(ДНК) живых организмом является предметом генетической инженерии.
Молекулы ДНК, создаваемые методами генетической инженерии, называют рекомбинантными. Раздел молекулярной биологии, связанный с созданием новых комбинаций генетического материала, способного обеспечивать биосинтез продуктов обмена веществ, получил название генетической инженерии.
Начало генетической инженерии было положено в 1972 году, когда американский ученый П. Берг в лабораторных условиях впервые создал рекомбинантную ДНК. Последняя соединила в себе фрагменты ДНК трех организмов: вируса «SV 40», бактериофага «лямбда» и бактерии «кишечная палочка» [1].
Опыт П. Берга был бы невозможен, если бы ранее не удалось открыть два уникальных типа ферментов: 1) рестриктазы, разрезающие молекулу ДНК в строго определенных участках; 2) лигазы, соединяющие отрезки различных молекул ДНК друг с другом. Рестриктазы получили весьма удачное образное название «биологических ножей», которыми манипулируют генные инженеры, разрезая молекулы ДНК на фрагменты.
Вторым необходимым условием успешного проведения опытов по генетической инженерии стало использование «векторов». Векторы представляют собой вирусы или получаемые из бактерий короткие вне хромосомные фрагменты их ДНК – плазмиды. С помощью рестриктаз и лигаз ученые встраивают в векторы необходимый фрагмент ДНК (ген). Задача вектора – внести новую ДНК (ген) в клетку и встроить ее в ДНК организма-хозяина.
Совершенствование методов генетической инженерии позволило объединять генетическую информацию неродственных организмов, в том числе стоящих на разных ступенях эволюции. Кроме того, «в пробирке» (in vitro)можно управлять процессом создания рекомбинантной ДНК так, чтобы обходить запрещающие механизмы живого организма. Методы генетической инженерии успешно внедряются в производство лекарственных препаратов.
На их основе уже производятся в широких масштабах инсулин, интерферон и интерлейкин.
На основе генетической инженерии разработаны технологии получения трансгенных растений (рис. 2) и животных, отличающихся не только высокой урожайностью (плодовитостью), но одновременно и повышенной устойчивостью к болезням и паразитам [7].

Рис. 2. Новые сорта кукурузы, полученные методом генетической инженерии.
Так, в Бельгии и США выведены сорта картофеля и томатов, которые устойчивы к колорадскому жуку и позволяют на 40-60% сократить применение инсектицидов [1].
3 Нанотехнологии для диагностики
С помощью нанотехнологии могут быть созданы чувствительные и чрезвычайно точные инструменты для диагностики с возможностями, находящимися далеко за пределами современного оборудования. Основная цель такой диагностики состоит в том, чтобы позволить врачам идентифицировать болезнь как можно раньше. Ожидается, что нанотехнология сделает возможным постановку диагноза на клеточном и даже субклеточном (органоидном) уровне.
Считается, что пероксид водорода — это только дезинфицирующее средство из домашней аптечки. Однако с помощью наночастиц оно может служить индикатором болезней в организме.
Созданы наночастицы органических красителей, способные обнаружить и определить количество пероксида водорода в организм ечеловека и животных. Эти наночастицы в будущем могут использоваться как простой и универсальный диагностический инструмент для обнаружения самых ранних стадий любой болезни, которая приводит к хроническому воспалению: от болезней сердца и артрита до рака и болезни Альцгеймера. Такие наночастицы невероятно чувствительны и позволяют обнаружить наномолярные концентрации пероксида водорода. Когда наночастица сталкивается с пероксидом водорода, агрегаты молекул красителя переходят в возбужденное состояние и испускают фотоны света, которые могут быть обнаружены простым детектором. Полимерная оболочка позволяет изолировать реагирующие вещества (пентацен и пероксид) в естественных условиях, но при этом расположить их всего в нескольких нанометрах один от другого[2].
Создан новый тип внутриклеточного наносенсора, который измеряет уровень клеточного pH (показатель кислотности среды).
В здоровых клетках этот показатель должен быть близок к значению, характерному для нейтральных растворов, — 7. Если рН сдвинут в кислую (ниже 7) или щелочную сторону (для клеток, как правило, выше 7,5), это свидетельствует о нарушении нормального состояния клетки. Внутриклеточный сенсор поможет быстро определить, здорова клетка или нет. Сенсор представляет собой иглу, на конце которой расположен зонд диаметром 1,4 мкм, состоящий из наностержней из ZnO диаметром 80…100 и длиной до900 нм (см. рис. 3) [3].

Рис. 3. Наносенсор
Наносенсор достаточно чувствителен для того, чтобы получать сигналы от отдельных органелл, чего ранее было невозможно достичь. Зонд не делает больших повреждений в клеточной мембране, что позволяет сохранить жизнеспособность клетки после измерений. Большие перспективы имеют экспресс-анализаторы, так называемые лаборатории на чипе. Примером такого оборудования может служить миниатюрный быстродействующий экспресс-анализатор, созданный учеными Калифорнийского университета, США (рис. 4).

Рис. 4. Экспресс-анализатор (http://www.nanonewsnet.ru).
Один чип размером 4×4 см, на котором размещены наноразмерные устройства, может заменить целый комплекс оборудования, необходимого для анализа ДНК / РНК, установления родства, определения генетически модифицированных организмов, ранней диагностики онкологических заболеваний, количественного определения белков и многого другого, при этом время анализа, занимавшего раньше несколько недель, сокращается до 15…30 мин [3].
4 Нанотехнологии и направленная доставка лекарств
В области терапии наиболее существенным результатом применения нанотехнологий является решение проблем направленной доставки препаратов и гипертермии онко тканей. Наночастицы позволяют доставлять лекарственные вещества точно к месту болезни, увеличивая эффективность и сводя к минимуму побочные эффекты; обеспечивают возможность контролируемого вывода терапевтических веществ и их метаболитов (продуктов превращения лекарств в ходе естественных процессов обмена веществ в организме). В этом направлении активно проводятся работы по созданию нанокапсул и наносфер для целенаправленной доставки лекарственных препаратов в организме человека (онкологическая, противогепатитная и антиВИЧ-терапия). Лекарства, содержащиеся внутри наночастиц, размер которых в 70 раз меньше, чем красные кровяные тельца, переносятся с током крови к определенному органу, где происходит пролонгированное выделение препарата. Для достижения эффективности лекарства необходимо, чтобы его молекулы попали к нужным клеткам: антидепрессанты — в мозг, противовоспалительные средства — в места воспалений, противоопухолевые препараты — в опухоль, не повреждая других органов. Для доставки лекарственных веществ непосредственно в больные органы и ткани могут быть использованы полимерные наноразмерные капсулы [2]. В настоящее время получены нанокапсулы со средним диаметром 10…5000 нм, включающие матрицу из воска или текстильного волокна и активного вещества. На рис. 5 представлена схема такой капсулы на основе природного биоконтейнера.
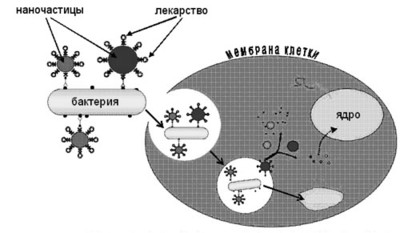
Рис. 5. Доставка наночастиц с лекарствами или фрагментами ДНК (генами) с помощью бактерии для лечения клеток(http://www.nanonewsnet.ru).
Адресная доставка наночастиц осуществляется двумя способами, получившими названия пассивного и активного нацеливания. Пассивное нацеливание основано на самопроизвольном накоплении наночастиц в очагах воспаления и тканях опухолей. Это возможно благодаря явлению ≪повышенной проницаемости сосудов≫. Стенка кровеносных капилляров в опухолях изменена так, что между ее клетками возникают поры (рис. 6) [1].
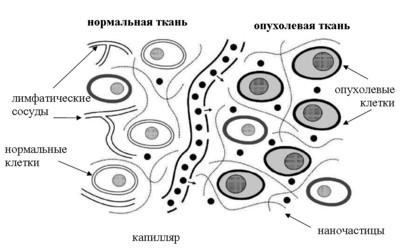
Рис. 6. Иллюстрация явления «повышенной проницаемости сосудов» в опухолевых тканях
Через них свободно проходят наночастицы, направляясь затем к клеткам опухоли. Из-за недоразвития лимфатических сосудов и недостаточного оттока межклеточной жидкости наночастицы накапливаются в опухолевой ткани (рис. 6) [1].
5 Медицинские имплантатына основе нанотехнологий
В современной медицинской практике все чаще используется «капитальный ремонт» или даже полная замена поврежденных органов. В ряде случаев для этого требуются сложнейшие искусственные материалы и конструкции, превосходящие по физическим свойствам естественные органы и структуры. Их разработка, испытание и применение стали предметом нового направления в медицине, возникшего на стыке медико-биологических и технических наук. Таким направлением является создание и использованием едицинских имплантатов.
Имплантаты – это специально создаваемые конструкции, которые вживляются в организм человека в роли заменителей отсутствующих или поврежденных органов (рис. 7). Они изготавливаются из биоматериалов –особых материалов, «уживающихся» с клетками и тканями организма.
$IMAGE7$
Рис. 7. Примеры имплантатов: А – дентальный имплантат; Б – костный имплантат (винты для фиксации позвоночника)
Среди современных металлических биоматериалов лидирующее положение занимает титан и создаваемые на его основе сплавы. Этот металл используется для изготовления протезов тазобедренных, коленных, челюстных суставов, пластин и спиц для костного сращивания, винтов для фиксации позвоночника [1].

Рис. 8. Имплантаты из наноструктурированного и обычного титана: а – стоматологические имплантаты фирмы Timplant (Чехия): NanoimplantR, d=2.4 mm; TimplantR, d =3.5 mm; б – имплантаты для коррекции позвоночника [1].
6 Тканевая инженерия
Восстановление поврежденных органов становится все более актуальным для современной медицины, привлекая внимание не только ученых-медиков и биологов, но и представителей технических наук. Как результат объединения их усилий оформилось новое межотраслевое направление– тканевая инженерия. Целью тканевой инженерии является конструирование компонентов биологических тканей для последующей имплантации в живой организм[1].
Технология получения тканевого имплантата включает:
1. Получение исходного клеточного материала. Для этого у пациента берут клетки той ткани, которая нуждается в восстановлении. Чаще всего отбирают неспециализированные (стволовые) клетки, которые лучше других размножаются в искусственной среде.
2. Изготовление биосовместимых конструкций (матриксов) для культивирования клеток пациента.
3. Формирование тканей в лабораторных условиях (in vitro). Стволовые клетки помещаются в специальную среду, которая способствует превращению их в клетки конкретного типа (рис. 9).
4. Имплантация полученных конструкций в организм пациента.
$IMAGE9$
Рис.9. Принцип тканевой инженерии
Важной задачей тканевой инженерии является конструирование трехмерных матриксов, способствующих образованию тканей. Матрикс должен выступать в качестве каркаса, а также стимула для размножения стволовых клеток и последующего превращения их в специализированные клетки новой ткани[1].
Ткань может быть выращена на матриксах, которые после имплантации в организм хозяина по мере роста новой ткани полностью растворяются.
При этом на месте дефекта остается только новая ткань. Возможно также имплантировать ≪биокомпозит≫, состоящий из матрикса и уже частично сформированной новой ткани [1].
7 Перспективные направление нанобиотехнологии
Нанобиотехнология – одна из самых перспективных технологий ХХІ столетия.
Ожидается, что нанобиотехнология инициирует инновации и сыграет важную роль в биомедицине, не только в областях транспорта лекарств и генной инженерии, а также в формировании изображений молекул, биомаркеров и биосенсоров [4]. Использование достижений нанотехнологии в медицине привело к появлению новой дисциплины, известной как наномедицина, которая включает процессы диагностики, лечения, профилактики заболеваний и травматических случаев, разработку обезболивающих средств, улучшение здоровья человека с использованием молекулярных приборов и молекулярных знаний о теле человека и создание отдельной отрасли медицины – клеточной инженерии.
Проблемы, которые решают ученые и инженеры в области нанобиотехнологии, имеют очень сложную природу, требуют создания материалов и устройств для влияния на субклеточном уровне с высокой степенью специфичности. Нанобиотехнология создает в первую очередь инструменты для наноманипуляций с наиболее важными биологическими макромолекулами ДНК, РНК и белками. Раньше для работы с ними требовалось огромное количество химических реакций. Проблема в том, что реакции происходят стохастически и можно измерить только средние значения величин. Для того, чтобы точно контролировать биологическую систему, необходимы инструменты, которые взаимодействуют с ней на наноуровне, в естественной среде обитания. Сначала интерес был сфокусирован на манипуляциях с ДНК, но сейчас разработаны методы манипуляции с белками, мембранами, клетками и т.д. [4].
Заключение
Нанотехнологии — символ начала XXI века для многих направлений развития науки, техники, технологий. Трудно назвать сферу знаний, отрасль промышленности, сельского хозяйства, медицины, в которой бы внедрение достижений нанотехнологий не оказало бы значительного влияния на увеличение эффективности производства. Для любого специалиста нанотехнологии — это создание систем, материалов, устройств, продуктов на наноразмерном уровне. Уже в ближайшие годы c применением достижений нанотехнологий следует ожидать существенных прорывов в науке, технике и технологии. К ним, в первую очередь, следует отнести значительное увеличение производительности компьютеров, восстановление человеческих органов, индивидуальный подбор и адресную доставку лекарств, получение новых материалов с неизвестными до настоящего времени свойствами, новые методы передачи информации, создание сверхминиатюрных устройств на основе самосборки и многое другое [5].
«Нанотехнологии произведут такую же революцию в манипулировании материей, какую произвели компьютеры в манипулировании информацией» Ralph Merkle (Xerox, Palo Alto).
Список литературы:
1. Сыч В.Ф., Дрождина Е.П., Санжапова А.Ф. Введение в нанобиологию и нанобиотехнологии. Учебное пособие для учащихся 10-11 классов средних общеобразовательных учреждений. - Спб.: образовательный центр «Участие», 2012 — 256 с.
2. Шабатина Т. И. Нанохимия и наноматериалы : учеб. пособие / Т. И. Шабатина, А. М. Голубев. - М.: Изд-во МГТУ им. Н. Э. Баумана, 2014. - 63 [1] с.
3. Сергеев Г.Б. Нанохимия. — 2-е изд., испр. и доп. — М.: Изд-во МГУ,2007. — 336 с.
4. Горобец С. В., Горобец О. Ю. Перспективы развития нанобиотехнологии// Химия, физика и технология поверхности. 2007. Вып 13. С.265-272
5. Эрлих Генрих Малые объекты — большие идеи. Широкий взгляд на нанотехнологии / Генрих Эрлих. —М. : БИНОМ. Лаборатория знаний, 2011. — 254 с.
Приложение 1.
Наноинженеру необходима клеточная и моллекулярная биология. Так как начальным (наиболее глубинным) уровнем организации живого является молекулярный. Структурно-функциональной единицей уровня является биомолекула (рис. 10), или молекула биополимера (молекула нуклеиновой кислоты, белка, полисахарида). На этом уровне осуществляются важнейшие процессы жизнедеятельности: хранение и передача наследственной информации, обмен веществ и энергии, дыхание и др. Из биомолекул формируются надмолекулярные структуры.
Субклеточный уровень рассматривается переходным между молекулярным и клеточным уровнями (рис. 10).
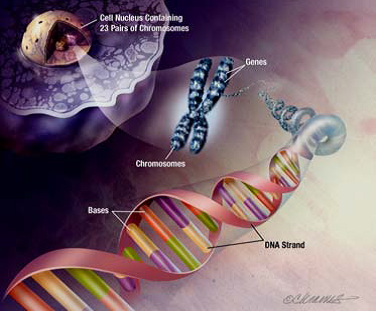
Рис.10. Биологические структуры, представляющие молекулярный (справа), субклеточный (посередине) и клеточный (слева) уровни организации жизни
Единицей уровня является надмолекулярная структура живой системы (элементарная биологическая мембрана, субчастица органоида, органоид). Процессы жизнедеятельности, протекающие на этом уровне, обеспечивают рост и специализацию клетки, самовосстановление и саморазрушение ее органоидов и др.
Клеточный уровень представлен клетками как самостоятельных организмов (бактерии, простейшие), так и клетками многоклеточных организмов.
Обладая способностью к биосинтезу, питанию, дыханию, развитию, размножению и т.п., клетка является основной структурой в организации живой природы.
Приложение 2.
1.Какова разрешающая способность светового и электронного микроскопов?
Обычно в световых микроскопах используются источники освещения в видимой области спектра (400-700 нм). Поэтому максимальное разрешение микроскопа не превышает 200-350 нм (0,2-0,35 мкм).
Реальное разрешение современных электронных микроскопов на практике составляет 0,1 – 0,7 нм, для биологических объектов – около 2 нм.
2. Что представляют собой биомакромолекулы?
Биомакромолекула – это гигантская молекула полимера (биополимера), построенная из многих повторяющихся единиц – мономеров. Существует три типа биомакромолекул: белки, нуклеиновые кислоты иполисахариды. Мономерами для них служат, соответственно, аминокислоты, нуклеотиды и моносахариды.
3. На каких уникальных свойствах ДНК основываются такие атрибуты живых организмов как наследственность и изменчивость?
Во-первых, молекула ДНК обладает способностью к самовоспроизводству. Единственный вид биологических макромолекул, которые могут воспроизводить себя путем самоудвоения – это молекулы ДНК. Благодаря этому ДНК выполняет ответственейшую миссию носителя наследственной информации во всех клеточных формах жизни.
Во-вторых, молекулы ДНК разных видов способны к гибридизации –слиянию отдельных цепочек ДНК от разных видов в единую двух цепочечную молекулу ДНК.
4. Объясните основные этапы выполнения генно-инженерной работы.
Каждая работа в области генетической инженерии выполняется в несколько этапов: 1) необходимый ген выделяют из естественных источников или синтезируют химическим путем; 2) подбирают вектор (молекулу ДНК, переносящую необходимый ген в клетку); 3) вектор и переносимый ген объединяют в единую структуру (рекомбинантную молекулу ДНК); 4) единую структуру, содержащую вектор и ген, вводят в клетку организма-хозяина. |