| Статистика |

Онлайн всего: 1 Гостей: 1 Пользователей: 0 |
|
Нанобиочипы: лаборатории на кристалле
Содержание
1. Введение. Понятие биочипа
2. Принцип работы биочипа
3. История биочипа
4. Нанобиочипы как основа медицины будущего
5. Заключение: перспективы развития биочипов
6. Список литературы (источники)
ВВЕДЕНИЕ. ПОНЯТИЕ БИОЧИПА
Биологические микрочипы являются одним из наиболее быстро развивающихся экспериментальных направлений современной биологии. Существует два основных типа биочипов. Первый тип - это микроматрицы различных соединений, главным образом биополимеров, иммобилизованных на поверхности стекла, в микрокаплях геля, в микрокапиллярах (рис. 1). Другим типом биочипов являются миниатюризованные "микролаборатории". Такой биочип представляет собой набор миниатюрных ячеек (микрочипов), расположенных на твердом субстрате (рис. 2), который позволяет проводить множество тестов, которые должны выполняться одновременно для достижения более высокой пропускной способности и скорости. Как правило, площадь поверхности биочипа не больше, чем ноготь. Как компьютерный чип, который может выполнять миллионы математических операций в секунду, биочип может выполнять тысячи биологических реакций, таких как декодирование генов, в течение нескольких секунд.

Рисунок 1. Сотни каплей геля, нанесенного на биочип
Пример второго типа биочипов: на поверхности ДНК-чипа нанесены олигонуклеотиды (рис. 2.) (короткий фрагмент ДНК или РНК). При добавлении анализируемого образца комплементарная таргетная ДНК в образце формирует дуплекс с олигонуклеотидом на чипе. В результате генерируется сигнал, свидетельствующий о наличии в пробе соответствующего объекта (инфекции, онкомаркера и т. п.).
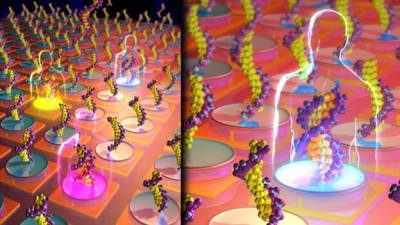
Рисунок 2. Олигонуклеотиды на поверхности биочипа
Биочипы помогли значительно ускорить идентификацию предполагаемых 80000 генов в ДНК человека, постоянному мировому научно-исследовательскому сотрудничеству, известному, как проект генома человека.
Также биочип используется в токсикологических, белковых и биохимических исследованиях. Биочипы также могут быть использованы для обнаружения в продуктах ГМО (Генетически модифицированный организм), для измерения количества глюкозы в крови или для быстрого обнаружения химических веществ, используемых в биологической войне, что позволит принять защитные меры.
ПРИНЦИП РАБОТЫ БИОЧИПА
Генетический код человека хранится в виде двойной спирали ДНК, образованной двумя полимерными цепями. Каждая из этих цепей представляет собой длинную последовательность, образованную из четырех нуклеотидов: аденина, гуанина, тимина и цитозина. При этом последовательность одной цепи однозначно определяет последовательность другой, поскольку нуклеиновые кислоты, расположенные на одинаковых позициях в разных цепях, являются комплементарными.
То есть если на сто тридцатой позиции в одной цепи находится аденин, то на той же позиции во второй цепи должен находится тимин, а если на двадцатой позиции во второй цепи стоит цитозин, то с полной уверенностью можно утверждать, что в первой цепи на двадцатом месте стоит гуанин. Когда две цепи объединяются в спираль, между комплементарными нуклеиновыми основаниями образуются водородные связи, которые и удерживают цепи вместе.
Именно на способности комплементарных оснований образовывать химические связи основан принцип действия биологических чипов. В ходе реакции происходит взаимодействие комплементарных цепей ДНК: одна из них (ДНК-проба) с известной последовательностью нуклеотидов зафиксирована на подложке (пластине), а другая одноцепочечная ДНК-мишень (зонд), меченная флуоресцентной меткой, вносится в ДНК-чип.
При взаимодействии биочипа с исследуемым образцом, предварительно обработанным светящимся (флуоресцентным) красителем, в соответствующих ячейках происходит химическая реакция, и тогда эти ячейки начинают светиться (рис. 3) - тем сильнее, чем интенсивнее процесс.
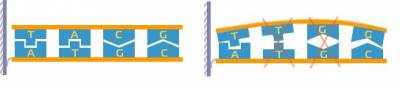
Рисунок 3. Справа выполняются условия молекулярной комплементарности – устойчивый комплекс.
Слева эти условия не выполняются – неустойчивый комплекс
Если соответствие между иммобилизованными молекулярными зондами и мечеными анализируемыми молекулами в растворе точно удовлетворяет условиям молекулярной комплементарности, то образующиеся комплексы будут термодинамически наиболее устойчивы.
В результате при определенных температурах их будет больше, чем комплексов, образованных с нарушением условий комплементарности, и, соответственно, совершенным комплексам будет отвечать более сильный сигнал флуоресценции. Совершенные и несовершенные комплексы, отвечающие специфическому и неспецифическому связыванию, обычно называют «перфектами» и «мисматчами».
Таким образом, определяются различные характеристики образца - например, присутствие в организме тех или иных возбудителей инфекций или, скажем, наличие в геноме каких-либо измененных генов.
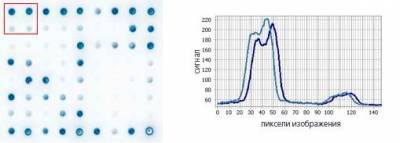
Флуоресцентное изображение микрочипа
Профиль флуоресцентного изображения микрочипа вдоль выбранных линий
ИСТОРИЯ БИОЧИПА
Разработка биочипов началась с сенсорных технологий. Один из первых портативных, химических датчиков был стеклянный электрод рН, изобретенный в 1922 году Хьюзом (Hughes, 1922). Так датчик K+ был изготовлен путем помещения в тонкую мембрану валиномицина (Schultz, 1996).
В 1953 году, Уотсон и Крик объявили о своем открытии в уже знакомой двойной спирали структуры ДНК молекул и заложил основу для генетических исследований, которые продолжаются до сегодняшнего дня (Nelson, 2000). Развитие методов секвенирования в 1977 году Гилбертом (Maxam, 1977) и Санджером (Sanger, 1977) (независимо друг от друга) позволило исследователям напрямую «читать» генетические коды, которые обеспечивают синтез белка. Это исследование показало, как гибридизация комплементарных отдельных олигонуклеотидных цепей могут быть использованы в качестве основы для зондирования ДНК. Еще два события открыли некоторые методы, используемые в современной ДНК-технологии. Так, в 1983 году Кэри Муллис открыл полимеразную цепную реакцию (ПЦР) (Nelson, 2000), позволяющую добиться значительного увеличения малых концентраций определённых фрагментов нуклеиновой кислоты (ДНК). Это открытие сделало возможным обнаружение чрезвычайно малых количеств ДНК в образцах. Во-вторых, в 1986 году Худ с помощниками разработали метод, маркирующий молекулы ДНК флуоресцентными метками, а не радиоактивными (Smith, 1986), что позволило оптически наблюдать процессы гибридизации.
На рисунке 5 показана схема стандартной платформы биочипа. Основные компоненты для зондирования – это микрочип, приёмник – для считывания информации с чипа, устройство обработки данных – для преобразования сигнала и вывода результатов.
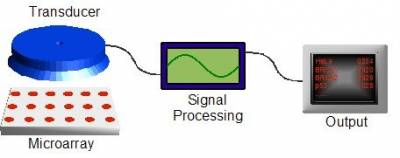
Рисунок 5. Схема стандартной платформы биочипа
НАНОБИОЧИПЫ КАК ОСНОВА МЕДИЦИНЫ БУДУЩЕГО
Сегодня ученые всего мира участвуют в амбициозной программе "Протеом человека", являющейся продолжением знаменитого "Генома человека".
Как известно, у человека 28 тысяч генов и все они расшифрованы. Но в то же время в нашем организме содержится 4,5 миллиона разных видов белков. Именно они регулируют функции различных органов, и сбои в их работе приводят к болезням. Цель программы "Протеом человека" - расшифровать, соотнести с генами и определить функции всех этих белков! Задача, прямо скажем, грандиозная. Дело не только в огромном количестве белков. Их концентрация в организме минимальна, буквально, считанные молекулы
Как известно, биочипы - это миниатюрные датчики, которые способны обнаружить исчезающие малые концентрации того или иного белка, гормона, ДНК или РНК. Сегодня эти устройства на основе иммуноферментного анализа применяются в медицине. Но метод довольно трудоемкий, так как связан с применением красителей, что сдерживает его широкое применение.
Разработка сибирских и московских ученых - следующий шаг в этой научной сфере. Ими созданы нанобиочипы, у которых принципиально иной принцип детекции - электронный. Сам датчик, процессоры, память - все это можно разместить в одном кристалле кремния. Сразу появляется возможность параллельно обрабатывать информацию, поступающую по десяткам тысяч каналов. Это настоящий прорыв по сравнению с нынешними биохимическими биочипами.
Кроме того, у нанобиочипов - рекордная чувствительность на уровне фемтомольных (10 в минус 15 степени) концентраций за счет того, что в качестве датчика используется транзистор в виде проволочки диаметром 10 нанометров.
ЗАКЛЮЧЕНИЕ: ПЕРСПЕКТИВЫ РАЗВИТИЯ БИОЧИПОВ
До появления технологии биологических микрочипов характерные размеры ячеек для анализа составляли ~0.1–1 см. Сокращение размеров ячеек до масштабов ~100 микрон в современной технологии биочипов существенно расширило возможности параллельного анализа (поскольку при заданных размерах чипа общее число ячеек растет обратно пропорционально квадрату размера ячейки), повысило его чувствительность и значительно сократило время диагностики. Массовое производство приведет к резкому уменьшению стоимости биочипов. Дальнейшее сокращение размеров ячеек позволит разместить на чипе размером 1x1 кв. см до миллиарда ячеек. Если считать, что на каждый из 30000 генов потребуется 40–50 ячеек, а каждая ячейка будет для контроля реплицирована 4 раза, то такие чипы позволят проводить параллельный анализ для геномов всех высших организмов. При этом техника измерений сигналов флуоресценции с таких чипов не требует кардинальных изменений. В более отдаленной перспективе возможна работа с группами из миллиона макромолекул в ячейке, что потребует совершенно иных методов измерения. Не исключено, что применение таких биочипов существенно выйдет за рамки биологических и медицинских приложений. Уже сейчас активно обсуждаются возможности применения, способности биологических молекул к специфичному молекулярному распознаванию для решения задач, требующих полного комбинаторного перебора вариантов. Активно изучаются также возможности использования способности биологических молекул к самосборке для создания регулярных наноструктур и наномеханических молекулярных устройств. Пока же биологические чипы помогают открывать новые гены, изучать систему регуляции генов, быстро проводить диагностику заболеваний и разрабатывать новые лекарства.
Список литературы:
1. www.bats.ch/bats/biosicherheit/blickpunkt/01-07_biochips.php
2. www.xvivo.net/illustration/bio-chip/
3. whatis.techtarget.com
4. www.biochip.ru.
5. en.wikipedia.org/wiki/Biosensor
6. en.wikipedia.org/wiki/Biochip
7. Главный редактор, академик РАН М.В. Алфимов – «Российские нанотехнологии», 2007 год.
8. www.infineon.com/cms/en/about-infineon/press/press-releases/2002/129911.html |
Категория: Наноинженерия (рефераты) | Добавил: ven6969 (22.12.2015)
| Автор: Ким Вениамин 
|
| Просмотров: 968
| Рейтинг: 0.0/0 |
Добавлять комментарии могут только зарегистрированные пользователи. [ Регистрация | Вход ] |
|