| Статистика |

Онлайн всего: 1 Гостей: 1 Пользователей: 0 |
|
Наноматериалы в медицине и биологии
Содержание
1. Введение
2. Понятия «нанотехнологии», «наноматериалы»
3) Разновидности наночастиц в биологии и медицине
4) Применение нанотехнологий в медицине: современное состояние
5) Наночастицы как лекарства
6) Наночастицы как контейнеры для доставки лекарств
7) Нанопоры для регистрации единичных олигонуклеотидов и секвенирования генома
8) Нанороботы, наноматериалы для тканевой биоинженерии, саморазмножающиеся геномы
9) Вывод
12) Список литературы
Введение
Большинство из нас не может представить себе жизнь без современных благ цивилизации, достижений науки, техники, медицины. Следующим шагом в этом развитии станет освоение нанотехнологий, в частности, систем очень малого размера, способных выполнять команды людей.
Технический прогресс направлен в сторону разработки более мощных, быстрых, компактных и изящных машин. Пределом такого развития можно считать машины, размером с молекулу. Машина, построенная из ковалентно связанных атомов, чрезвычайно прочна, быстра и мала. Разработкой, созданием и управлением такими машинами занимается молекулярная нанотехнология. Эта отрасль открывает невиданные ранее, фантастические перспективы взаимодействия человека с миром.
Разновидности наночастиц в биологии и медицине
Формальными признаками наночастиц являются сферическая форма и размер от 1 до 250-300 нм. В связи с этим, в группу наночастиц относят весьма разнородные по химическому строению и физическим свойствам частицы (табл. 1).
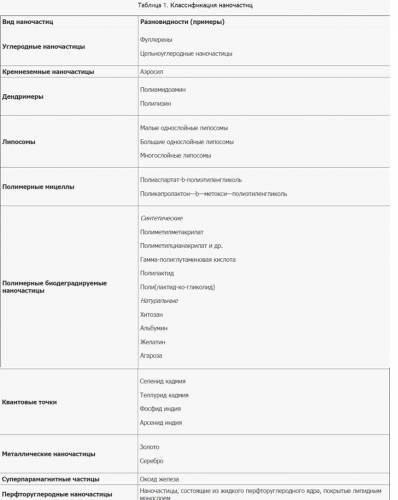
Применение нанотехнологий в медицине: современное состояние
Термин нанотехнологии убедительно входит в нашу жизнь. В 1959 г. известный американский физик-теоретик Ричард Фейнман говорил о том, что существует "удивительно многосложный мир малых форм, а когда-нибудь люди будут удивляться тому, что до 1960 г. ни один человек не относился всерьез к изучениям этого мира". На начальном этапе развитие нанотехнологии определялось главным образом разработкой устройств зондовой микроскопии. Эти аппараты являются как бы глазами и руками нанотехнолога.
Прогресс в сфере нанотехнологии на данный момент связан с созданием наноматериалов для аэрокосмической, автомобильной, электронной промышленности.
Но постепенно все чаще отмечается как многообещающая область использования нанотехнологии – медицина. Это вызвано тем, что новая технология позволяет работать с веществом в масштабах, еще недавно казавшихся фантастическими – микрометровых, и даже нанометровых. Как раз такие величины типичны для главных биологических структур - клеток, их компонентов (органелл) и молекул.
Сегодня можно утверждать о возникновении нового направления - наномедицины. Впервые мысль об использовании микроскопических устройств в медицине была высказана в 1959 г. Р. Фейнманом в своей знаменитой лекции "Там внизу - много места" (со ссылкой на идею Альберта Р. Хиббса). Но всего лишь в последние несколько лет идеи Фейнмана приблизились к реальности.
Сейчас мы еще довольно далеки от описанного Фейнманом микроробота, способного через кровеносную систему попасть внутрь сердца и сделать там операцию на клапане. Современные приложения нанотехнологий в медицине можно разделить на несколько групп: Наноструктурированные материалы, в т. ч., поверхности с нанорельефом, мембраны с наноотверстиями; Наночастицы (в т.ч., фуллерены и дендримеры); Микро- и нанокапсулы; Нанотехнологические сенсоры и анализаторы; Медицинские применения сканирующих зондовых микроскопов; Наноинструменты и наноманипуляторы; Микро- и наноустройства различной степени автономности.
Американская компания C-Sixty Inc. Проводит предклинические испытания средств на основе фуллереновых наносфер С60 с упорядоченно расположенными на их поверхности химическими группами. Эти группы могут быть подобраны таким образом, чтобы связываться с заранее выбранными биологическими мишенями. Спектр возможных применений чрезвычайно широк. Он включает борьбу с вирусными заболеваниями такими, как грипп и ВИЧ, онкологическими и нейродегенеративными заболеваниями, остеопорозом, заболеваниями сосудов. Например, наносфера может содержать внутри атом радиоактивного элемента, а на поверхности - группы, позволяющие ей прикрепиться к раковой клетке.
Подобные разработки проводятся и в России. В Институте экспериментальной медицины (Санкт-Петербург) использовали аддукт фуллерена с поливинилпирролидоном (ПВП). Это соединение хорошо растворимо в воде, а полости в его структуре близки по размерам молекулам С60. Полости легко заполняются молекулами фуллерена, и в результате образуется водорастворимый аддукт с высокой антивирусной активностью. Поскольку сам ПВП не обладает антивирусным действием, вся активность приписывается содержащимся в аддукте молекулам С60.
В пересчете на фуллерен его эффективная доза составляет примерно 5 мкг/мл, что значительно ниже соответствующего показателя для ремантадина (25 мкг/мл), традиционно используемого в борьбе с вирусом гриппа. В отличие от ремантадина, который наиболее эффективен в ранний период заражения, аддукт С60/ПВП обладает устойчивым действием в течение всего цикла размножения вируса. Другая отличительная особенность сконструированного препарата - его эффективность против вируса гриппа
А- и В-типа, в то время как ремантадин действует только на первый тип.
Наносферы могут использоваться и в диагностике, например, как рентгеноконтрастное вещество, прикрепляющееся к поверхности определенных клеток и показывающее их расположение в организме.
Особый интерес вызывают дендримеры. Они представляют собой новый тип полимеров, имеющих не привычное линейное, а ветвящееся строение.
Собственно говоря, первое соединение с такой структурой было получено еще в 50-е годы, а основные методы их синтеза разработаны в основном в 80-е годы. Термин "дендримеры" появился раньше, чем "нанотехнология", и первое время они между собой не ассоциировались. Однако последнее время дендримеры все чаще упоминаются именно в контексте их нанотехнологических (и наномедицинских) применений.
Это связано с целым рядом особых свойств, которыми обладают дендримерные соединения. Среди них: предсказуемые, контролируемые и воспроизводимые с большой точностью размеры макромолекул; наличие в макромолекулах каналов и пор, имеющих хорошо воспроизводимые формы и размеры; способность к высокоизбирательной инкапсуляции и иммобилизации низкомолекулярных веществ с образованием супрамолекулярных конструкций "гость-хозяин".
Наночастицы как лекарства
В период 1998-2005 г.г. опубликовано более 200 научных работ, демонстрирующих эффективность применения фуллеренов при лечении целого ряда заболеваний, включая рак, склероз, вирусные и бактериальные инфекции (менингит и ВИЧ). В России ведутся работы и получены положительные результаты, подтвержденные публикациями и патентами, в области применения фуллеренов и их модификаций для лечения гриппа, онкологических заболеваний и бактериальных инфекций (туберкулез). Получены данные о возможности использования наночастиц для производства эффективных вакцин.
Разнообразие технологий производства фуллеренов и их производных позволяет планировать существенное расширение спектра применения наночастиц как лекарств. Лекарства в виде наночастиц обладают целым рядом преимуществ: высокой скоростью растворения, повышенной биодоступностью, быстрым терапевтическим эффектом, снижаются риски развития побочного действия.
Наши исследования на протяжении тридцати лет привели к созданию нанолекарства – препарата «ФОСФОГЛИВ». Также разработана инъекционная форма лекарственного препарата «ФОСФОГЛИВ» с использованием наночастиц.
Наносистема лекарственного средства ФОСФОГЛИВ представляет собой частицы диаметром не более 50 нм и содержит соевый фосфатидилхолин и глицирризиновую кислоту. При клиническом применении препарата отмечается его ингибирующее действие на репликативную активность вирусов гепатита В и С, а также положительное влияние на иммунный интерфероновый статус. Ремиссия при лечении гепатита С с использованием препарата составила 70%. «ФОСФОГЛИВ» обладает очень низкой токсичностью, не вызывает аллергических реакций, устойчив при хранении. Получают препарат эмульгированием активных компонентов в водном растворе мальтозы под давлением 1500 атм. Потом следуют процессии ультрафильтрации и лиофилизации раствора в флаконах.
Получено также изображение частиц препарата с помощью АСМ. Основная масса частиц имеет размеры около 40 нм.
Сейчас ФОСФОГЛИВ – сертифицированный лекарственный препарат из группы гепатопротекторов, обладает также противовирусной активностью.
Фосфатидилхолин в составе средства, действуя наподобие «мембранного клея», восстанавливает структуру поврежденных мембран гепатоцитов, восстанавливая функцию печени. Глицирризиновая кислота в виде натриевой соли подавляет репродукцию вируса в печени и других органах за счет стимулирующего действия на продукцию интерферона, увеличения активности естественных киллеров и др. Препарат показан при острых и хронических гепатитах (А, B, C и D), дегенеративных изменениях печени, при лекарственном и алкогольном поражении печени, при псориазе, экземе и бронхиальной астме.
Наночастицы как контейнеры для доставки лекарств
Помимо создания новых лекарственных форм многие разработки идут по пути конструирования наносистем, способных доставлять лекарство непосредственно к органам и клеткам-мишеням. Улучшенный транспорт лекарств в очаг развития патологического процесса позволяет добиться повышения эффективности уже существующей лекарственной терапии. Объем продаж в США лекарств с системой улучшенной доставки в настоящее время составляет 20% от общего объема рынка фармпрепаратов В России разработки систем адресной доставки ведутся по двум направлениями: пассивный направленный транспорт (облегченное проникновение естественных барьеров) и специфическая доставка («узнавание» патологической ткани), что отвечает мировому уровню развития исследований в этой области. Практические результаты уже в ближайшее время могут быть достигнуты в области использования фосфолипидных частиц, липосом и фуллеренов в качестве контейнеров для доставки препаратов (в. т.ч. и вакцин).
Лекарства, снабженные системой доставки, имеют ряд преимуществ по сравнению со свободными препаратами: а) повышается растворимость гидрофобных лекарств; б) улучшается их проникновение в клетки; в) улучшается фармакокинетика, г) у многих лекарств появляется способность пересекать мембранные и гематоэнцефалический барьеры. Использование наносистем для транспорта лекарственных препаратов позволяет не только увеличить биодоступность последних, но и обеспечить поступление препарата в определенные органы и клетки-мишени.
За последние 20 лет наиболее достигнуты существенные успехи в разработке фосфолипидных транспортных систем. Так, фосфолипидные наночастицы (мицеллы/ липосомы) до сих пор имеют ряд преимуществ перед другими, например, полимерными наночастицами. Они нетоксичны, биодергадируемы, не вызывают аллергических реакций, благодаря своему строению и составу, имеют высокое сродство к мембранам клеток, что позволяет доставлять лекарство внутрь клетки. В настоящее время в мире существует 10-15 сертифицированных наносистем, используемых в качестве переносчиков лекарств, а на фармацевтическом рынке – несколько десятков препаратов, в основном, противоопухолевых, снабженных фосфолипидной системой транспорта (липосомы), например: дауномицин и доксорубицин (2005), винкристин (2006), аннамицин и третиноин (2005). Большинство препаратов находятся на последних стадиях клинических испытаний.
Высокую транспортную эффективность показала и наша разработка транспортной системы [Ipatova et al., 2006] – фосфолипидная наносистема «Нанофосфолип», представляющая собой стабильный при хранении лиофильно высушенный порошок фосфолипидных наночастиц, диаметром 20-30 нм.
Такие наноконтейнеры лекарств хранятся до 5 лет без потери фармакологических свойств, обладают большей биодоступносью, слабо поглощаются ретикулоэндотелиальной системой клеток, фармакодинамика их в 2-3 раза лучше, чем у липосом сложного состава.
НАНОФОСФОЛИП как транспортную систему можно наполнять различными лекарственными субстанциями:
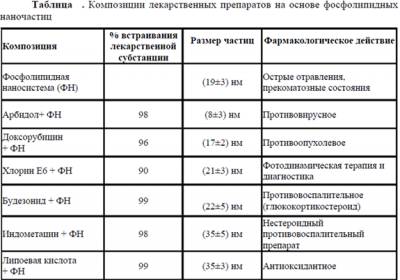
Уже проведено сравнительное исследование фармакологического эффекта на крысах при пероральном введении крысам с вирусом гепатита А свободной лекарственной формы Арбидола и в составе фосфолипидных наночастиц (Арбидол- НФ). Показано увеличение концентрации Арбидола-НФ в крови в несколько раз по сравнению со свободным Арбидолом через 15 мин после приема препарата внутрь и его эффективное ингибирующее действие на репродукцию вируса гепатита А в более низких дозах, чем свободный Арбидол.
Нанопоры для регистрации единичных олигонуклеотидов и секвенирования генома
Развитие персонифицированной медицины напрямую связано с информацией о геноме человека. Для расшифровки генома в 1990 году правительство CllIA
санкционировало проект «Геном человека». Стоимость секвенирования генома примата составляет порядка 20 млн. долларов и занимает по времени 3-5 месяцев. Для удешевления процедуры секвенирования генома человека до порядка1000 долларов был открыт проект "Персональный геном", инициированный Гарвардской медицинской школой [www.mcb.harvard.edu/branton/projects-NanoporeSequencing.htm].
Осуществить это можно с применением новых методов секвенирования генома. Одним из наиболее перспективных методов идентификации нуклеиновых оснований в молекуле ДНК может стать метод, основанный на использовании физических различий между четырьмя нуклеотидами. Эти различия можно выявить, протягивая ДНК через нанопору, и регистрируя при этом электрический сигнал, возникающий в электронной структуре нанопоры. Такой метод не предполагает использования процедуры амплификации, что значительно удешевляет технологию секвенирования до 1000 долларов за сутки и повышает быстродействие процедуры. Согласно оценкам исследователей из Гарвардского Университета, первый шаг в создании такой технологии сделан: создано устройство на основе нанопор, регистрирующие отдельные олигонуклеотиды. В устройстве счета единичных олигонуклеотидов регистрируется изменение во времени электрического сопротивления нанопоры с диаметром порядка нескольких нанометров при прохождении через нее ДНК. К сожалению, пока исследователи имеют затруднения в тестировании последовательности оснований, так как ДНК совершает обратные движения, как бы танцует. Решение разрабатывается с использованием электрического поля для удержания движения ДНК под контролем.
Такой подход необходимо развивать и в нашей стране, так как это дает возможность сконструировать портативные, относительно дешевые,
быстродействующие наноустройства для секвенирования генетического материала. Эти устройства найдут применение и в решении проблем медицинской диагностики, и в анализе продуктов на наличие генетически-модифицированного материала.
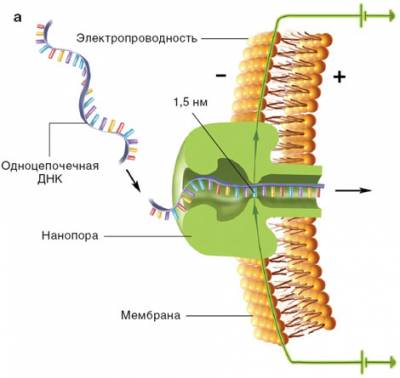
Нанороботы, наноматериалы для тканевой биоинженерии, саморазмножающиеся геномы
Изначально (1959) концепция наномедицины возникла из фантастических идей создать и внедрить в тело человека крошечные нанороботы и родственные им механизмы, которые выполняли бы «ремонт» клеток на молекулярном уровне [www.zyvex.com/nanotech/Feynman.html].
Например, механический наноробот помещается в кровяное русло, направляется в сердце, «осматривает» его, находит поврежденный клапан и с помощью микроскальпеля оперирует. Другая возможность - микроробот – помещается в организм пациента, находит и уничтожает больные клетки.
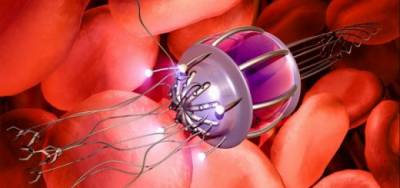
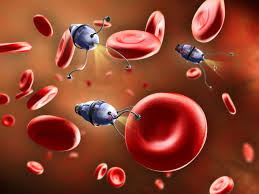
Медицинские нанороботы являются кибернетическими устройствами нанометрических размеров, изготовленные с атомарной точностью. Медицинские нанороботы способны функционировать в организме человека производя контролируемую коррекцию молекулярных и клеточных процессов.
В настоящее время, не существует теоретических барьеров, препятствующих созданию такого рода устройств с широким спектром функций. Современный уровень развития нанотехнологии позволяет практически конструировать работоспособные медицинские нанороботы, в частности, устройства для контроля уровня глюкозы в крови (перспективы использования - при мониторинге диабетических больных) и для вырабатывания инсулина. В то же время, методами молекулярного моделирования продемонстрированы возможности создания на порядок более сложных систем: искусственных фагоцитов, эритроцитов и т.п.
Если усилия нанобиотехнологии направлены на то, чтобы создавать новые методы диагностики, новые транспортные системы и новые лекарства, то в наномедицине на первое место выходят медицинские нанороботы, наноматериалы для тканевой биоинженерии, и саморазмножающиеся геномы.
Особые свойства наноматериалов могут быть использованы для выращивания искусственных органов и тканей. За рубежом разработана на сегодняшний день методика восстановления хрящевой ткани, которая по механическим и биохимическим свойствам была близка к естественному хрящу. В России задел в этом направлении сделан в области использования биосовместимых наноматериалов для восстановления механических свойств зубной эмали.
Самовоспроизводящиеся геномы представляют собой минимальные
искусственные биосистемы, способные самостоятельно выполнять лишь одну базовую функцию – воспроизводить себя. Технологии живых систем перспективны с точки зрения контролируемого создания наноустройств различного назначения. Принципиально важной особенностью биологических систем является способность к самовоспроизведению.
В России имеется необходимая компонентная база и коллективы с опытом синтеза (конструирования) олигонуклеотидных конструкций для начала работ по созданию минимальной искусственной биосистемы.
Начало 2008 года ознаменовалось мировой сенсацией – Крейгу Вентеру и Клайду Хатчисону удалось синтезировать первый в мире искусственный геном. Это был геном паразитической бактерии Mycoplasma genetalium, состоящий всего! из 485 генов. Процесс синтеза очень сложный и многоступенчатый: сначала синтезируются олигонуклеотиды, затем из них формируются фрагменты генома с помощью реакций лигирования и полимеразной цикличной сборки, и, наконец, собирается полный геном. Внедрение же этого искусственного генома в бактериальную клетку без генетического аппарата привело к созданию следующей сенсации – искусственной бактерии Mycoplasma laboratorium. Искусственный геном заработал! Т.е. впервые за всю историю науки синтезирована живая система.
Создание синтетического генома позволит лучше понять, как он работает, как взаимодействуют гены в составе полного генома. Станет возможным проследить, как эволюционирует сложный геном. В биотехнологии возможна будет манипуляция отдельными генами микроба-продуцента, можно будет создать геном, направленный на синтез нужного вещества (например, антибиотика). Здесь на ум приходят слова: “ОКОЛО 10 000 ЛЕТ ТОМУ НАЗАД ЧЕЛОВЕК НАЧАЛ ОДОМАШНИВАТЬ РАСТЕНИЯ И ЖИВОТНЫХ. СЕЙЧАС НАСТУПИЛО ВРЕМЯ ОДОМАШНИВАТЬ МОЛЕКУЛЫ.” (Lindguist S., 2003, Engineering and Medicine, Crete, Greece, 1-5).
Вывод
Внедрение нанотехнологий в биологию и медицину способно существенно расширить возможности применения конкурентоспособных результатов исследований в медицине, фармакологии, сельском хозяйстве уже в самом ближайшем будущем. На это направлена и Национальная доктрина развития в Российской Федерации нанотехнологий, принятая в 2006 году.
Мировые инвестиции в сферу разработки нанотехнологий значительно возрастают из года в год. В США национальная доктрина в области нанобиотехнологий включает создание высокочувствительных нанодетекторов для выявления заболеваний на ранней стадии. Предполагаемый рынок нанотехнологического оборудования для медицины в США на базе электронных и атомно-силовых микроскопов составит порядка 5 млрд. долларов.
В настоящее время в России ведутся работы по созданию современной инфраструктуры и реализации потенциала отечественной наноиндустрии. Так, в 2007 году создана Государственная корпорация «Российская корпорация нанотехнологий» (РОСНАНОТЕХ), которая должна содействовать реализации государственной политики в сфере нанотехнологий, развитию инновационной инфраструктуры в сфере нанотехнологий, реализации проектов создания перспективных нанотехнологий и наноиндустрии. Утверждена Федеральная целевая программа «Развитие инфраструктуры наноиндустрии в Российской Федерации на 2008—2010 годы». Объём финансирования в рамках программы — 27,7 млрд.рублей. Программой назначены головные организации отраслей по направлениям развития нанотехнологий, в частности по направлению «Нанобиотехнологии» головной организацией назначен
Российский научный центр «Курчатовский институт». В сентябре 2007 года Минпромэнерго РФ утвердило масштабную программу развития электронной промышленности страны до 2025 года, в рамках которой предусматриваются инвестиции на общую сумму около 250 млрд. руб., существенная часть которых будет израсходована на создание прорывных технологий, и в частности, нанотехнологий.
Какой будет нанобиотехнология в нашем мире? Как отразятся ее прорывные и фантастические сегодня разработки на здоровье и благополучии нашей цивилизации? Как они изменят нас, наше отношение к жизни и к планете? Ответы на эти вопросы определят стратегические направления развития нанотехнологий, а в более широком контексте – и цивилизации XXI века вообще.
«ДЕЙСТВИТЕЛЬНОСТЬ В ТОМ, ЧТО НАНОТЕХНОЛОГИЯ УЖЕ РЕАЛЬНОСТЬ СЕГОДНЯШНЕГО ДНЯ» (R.F.Serfice, Science (2004), 304, 1732-1734).
Таким образом, нанотехнологии, как и информационные технологии, призваны изменить наши представления об окружающем мире. Одна их основных задач нанотехнологий – заполнить ту пропасть, которая существует между ЖИВОЙ природой и НЕЖИВОЙ. Вероятно, только с помощью этой науки мы в состоянии понять их принципиальные отличия. В тоже время, уже существующие в настоящем времени достижения нанотехнологий – это создание синтетических саморазмножающихся геномов и появившаяся в прошлом году синтетическая клетка микоплазмы – Mycoplasma laboratorium (Институт Крейга Вентера, США), – позволяют надеяться на то, что казавшаяся непреодолимой эта пропасть в ближайшем будущем будет преодолена. Поэтому не вызывает никакого сомнения, что нанобиотехнология и наномедицина – это науки, которые составляют основу биомедицины начала 21-го столетия.
Список литературы
1. Рыбалкина М. Нанотехнологии для всех. Большое в малом. – М.: 2005. – 444 с.
2. Губин, С. П. Магнитные наночастицы: методы получения, строение, свойства / Ю. А. Кокшаров, Г. Б. Хомутов, Г. Ю. Юрков. // Успехи Химии. - 2005. - Т.74. - № 6. - С. 539-574.
3. Дыкман, Л. А. Золотые наночастицы: синтез, свойства, биомедицинское применение / Л. А. Дыкман. – М. : Наука, 2008. – 319 с.
4.
5. Ерофеев, Н. П. Наноструктуры: физическая сущность и варианты применения в медицине / Н. П. Ерофеев, Г. Г. Зегря, Д. Б. Вчерашний // Успехи химии. – 2011. - № 8. – С. 48-53.
6. Полянский, А. А. Наномедецина будущего: Трансдермальная доставка с использованием наночастиц / А. А. Полянский // Молекула. Взгляд изнутри. – 2008. - № 10. – С. 72-79
7. Балабанов, В. И. Нанотехнологии. Наука будущего / В. И. Балабанов - М. : Эксмо, 2009 г. - 256 с.
8. Петрищев, Н. П. Направленная доставка лекарственных препаратов в поврежденные ткани с использованием наноразмерных частиц / Н. П. Петрищев, М. М. Галагудза, С. М. Минасян, Д. В. Королев // Химическая физика. – 2009. - № 2. – С. 92-98.
9. Власов Г. П. Эволюция методологии создания биодеградирующих и биосовместимых полимерных носителей биологически активных веществ. В книге “Нанотехнологии в медицине и биологии” (Под ред.Е.В.Шляхто). СПб.: Издательство ”Любавич”, 2009. С.137-166.
10. . Иванов Ю.Д., Гнеденко О.В., Николаева Л.И., Конев В.А., Ковалев О.Б.,Учайкин В.Ф., Говорун В.М., Покровский В.И., Арчаков А.И. (2003) Микробиол., эпидемиолог. и иммунолог., №2, 58-62.
11. Дмитриев Д.А., Массино Ю.С., Сегал О.Л., Смирнова М.Б., Павлова Е.В.,Коляскина Г.И., Гуревич К.Г., Гнеденко О.В., Иванов Ю.Д., Арчаков А.И., Осипов А.П., Дмитриев А.Д., Егоров А.М. (2002) Биохимия, 67, 1356-1365.
12. Yamamoto Y., Miura T., Teranishi T., Miyake M., Hori H., Suzuki M.,Kawamura N., Miyagawa H., Nakamura T., Kobayashi K. (2004) Phys. Rev. Lett., 93, 116801.
13. Anderson N.L. and Anderson N.G. (2002) Molecular &Cellular Proteomics 845-867.
14. Cush R., Cronin J.M., Stewart W.J., Maule C.H., Molloy J., Goddard N.J. (1993) Biosensor and Bioelectronics., 8, 347-353. |
| Категория: Наноматериалы и нанотехнологии (курсовые работы магистров РУДН) | Добавил: sashashvetsov3 (21.12.2015)
| Автор: Швецов А.О.
|
| Просмотров: 3317
| Рейтинг: 0.0/0 |
Добавлять комментарии могут только зарегистрированные пользователи. [ Регистрация | Вход ] |
|